摘要:钛和钛的合金已被广泛用于制造电讯器材.人造骨骼.化工设备.飞机等航天航空材料.被誉为“未来世界的金属 .试回答下列问题:
网址:http://m.1010jiajiao.com/timu_id_174566[举报]
TiO2在很多领域有着广泛的应用前景.
(1)制备TiO2的常见方法:将TiCl4水解产物加热脱水生成TiO2.已知常温下Ti(OH)4的Ksp=7.94×10-54,测得TiCl4水解后溶液的pH=2,则此时溶液中c(Ti4+)= .
(2)制备纳米TiO2的方法:以N2为载体,用钛醇盐Ti(OR)4和水蒸气反应生成Ti(OH)4,再控制温度生成纳米TiO2.温度控制不当会使产物含结晶水,测定产物aTiO2?bH2O组成的方法如下:
步骤一:取样品2.010g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液.
步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用0.1000mol?L-1NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+.重复滴定2次.滴定所得的相关数据如表:
①钛醇盐Ti(OR)4和水蒸气反应的化学方程式为 .
②步骤一中用稀硫酸而不用水定容的原因是 .
③通过计算确定该样品的组成 (写计算过程).
查看习题详情和答案>>
(1)制备TiO2的常见方法:将TiCl4水解产物加热脱水生成TiO2.已知常温下Ti(OH)4的Ksp=7.94×10-54,测得TiCl4水解后溶液的pH=2,则此时溶液中c(Ti4+)=
(2)制备纳米TiO2的方法:以N2为载体,用钛醇盐Ti(OR)4和水蒸气反应生成Ti(OH)4,再控制温度生成纳米TiO2.温度控制不当会使产物含结晶水,测定产物aTiO2?bH2O组成的方法如下:
步骤一:取样品2.010g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液.
步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用0.1000mol?L-1NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+.重复滴定2次.滴定所得的相关数据如表:
| 滴定 序号 |
待测液体积/mL | NH4Fe(SO4)2标准溶液 滴定管起点读数/mL |
NH4Fe(SO4)2标准溶液 滴定管终点读数/mL |
| 1 | 25.00 | 0.02 | 24.02 |
| 2 | 25.00 | 0.08 | 24.06 |
| 3 | 25.00 | 0.12 | 24.14 |
②步骤一中用稀硫酸而不用水定容的原因是
③通过计算确定该样品的组成
(08鄞州中学月考)金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为: aTiO2 + bCl2 + cC ![]() aTiCl4 + cCO ……反应①
aTiCl4 + cCO ……反应①
TiCl4 +2Mg ![]() Ti + 2MgCl2 ……反应②
Ti + 2MgCl2 ……反应②
关于反应①、②的分析不正确的是 ( )
① TiCl4在反应①中是还原产物,在反应②中是氧化剂;② C、Mg在反应中均为还原剂,被还原;③ 在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;④ a=1,b=c=2;⑤ 每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②⑤
查看习题详情和答案>> (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
A.钙钛矿的化学式可表示为![]()
B.钙钛矿晶体中与1个Ca2+距离最近且等距离的O2-有6个
C.太阳能光催化裂解水制氢气的反应可表示为:![]()
D.太阳能光催化裂解水制氢气的反应为放热反应
查看习题详情和答案>>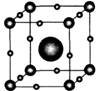 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )