摘要:12.有酸HA和碱BOH两种溶液.下列说法正确的是 ( ) A.相同条件下.相同浓度的HA和BOH溶液.前者的c(H+)与后者的c(OH-)一定相等 B.等浓度.等体积的HA与NaA混合.溶液一定呈酸性 20090520 C.HA和BOH混合.溶液中微粒浓度关系可能为 c(A-)>c(B+)>c(OH-)>c(H+) D.室温下.向lmL pH=l的HA溶液中加水至10mL.则所得溶液中水电离出的c(H+)≤1.010-12mol·L-1
网址:http://m.1010jiajiao.com/timu_id_1745464[举报]
航天技术上使用的氢-氧燃料电池具有高能、轻便和不污染环境等优点.氢-氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式可表示为2H2+O2=2H2O.酸式燃料电池的电解质是酸,其负极反应可表示为:2H2-4e-=4H+,则其正极反应式可表示为:
查看习题详情和答案>>
O2+4H++4e-═2H2O
O2+4H++4e-═2H2O
;放电一段时间后电解质溶液的pH将变大
变大
(填“变大、变小、不变”)碱式氢-氧燃料电池中的电解质是碱,其正极反应式为:O2+2H2O+4e-=4OH-,则其负极反应可表示为:2H2+4OH--4e-=4H2O
2H2+4OH--4e-=4H2O
.
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:
①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在110mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,然后加入蒸馏水,定容,使液面恰好与刻度相切;
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
(1)有500mL、250mL、150mL的量筒备用,应选用量程为 的量筒,理由是 ;
(2)有酸式和碱式两种滴定管备用,该实验应选用 ,理由是 ;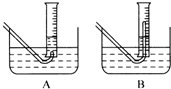
(3)在步骤③测量气体体积时,必须待试管和量筒内的气体都冷却到室温时进行,应选用右图装置中 ,理由是 ;此时量筒内的液面高于水槽中液面,立即读数会使Na2O2的纯度 (填“偏高”“偏低”或“不变”);应进行的操作是 ;
(4)在步骤⑤中滴定达到终点时,溶液的颜色变化是 ;
(5)该过氧化钠的纯度为 (实验中得到的气体体积均看作为标准状况下).
查看习题详情和答案>>
①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在110mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,然后加入蒸馏水,定容,使液面恰好与刻度相切;
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
(1)有500mL、250mL、150mL的量筒备用,应选用量程为
(2)有酸式和碱式两种滴定管备用,该实验应选用

(3)在步骤③测量气体体积时,必须待试管和量筒内的气体都冷却到室温时进行,应选用右图装置中
(4)在步骤⑤中滴定达到终点时,溶液的颜色变化是
(5)该过氧化钠的纯度为
 (1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O=4Al(OH)3,负极为:
(1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O=4Al(OH)3,负极为:Al
Al
,负极发生:氧化
氧化
反应(填“氧化”或“还原”);正极为铂网,电流
电流
(填“电子”或“电流”)从铂极流出;海水为电解质溶液,海水中的Na+移向正极
正极
(填“正极”或“负极”).若电路中转移3mol电子,则负极材料质量减少
27
27
克(2)航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2=2H2O.酸式氢燃料电池的电解质是酸、其负极反应为:2H2-4e-=4H+,则正极反应为
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
;碱式氢氧燃料电池的电解质是碱,其正极反应表示为:O2+2H2O+4e-=4OH-,则负极反应为:
2H2-4e-+4OH-=4H2O
2H2-4e-+4OH-=4H2O
.(3)如右图:若A为铜片,B为铁片,电解质为FeCl3溶液,则作铜片为
正
正
极(填正或负),写出电极反应式:正极2Fe3++2e-=2Fe2+
2Fe3++2e-=2Fe2+
负极Fe-2e-=Fe2+
Fe-2e-=Fe2+
.(1)我国首创的海洋电池,总反应为:4Al+3O2+6H2O═4Al(OH)3,负极为
(2)航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2═2H2O.酸式氢氧燃料电池的电解质是酸,其负极反应为:2H2-4e-═4H+,则正极反应为
(3)蓄电池Pb+PbO2+2H2SO4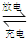 2PbSO4+2H2O放电时,正极电极反应式
2PbSO4+2H2O放电时,正极电极反应式
查看习题详情和答案>>
Al
Al
,负极发生氧化
氧化
反应(填“氧化”或“还原”),负极反应Al-3e-=Al3+
Al-3e-=Al3+
;正极为铂网,电流
电流
(填“电子”或“电流”)从铂极流出;海水为电解质溶液,海水中的Na+移向正极
正极
(填“正极”或“负极”).(2)航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2═2H2O.酸式氢氧燃料电池的电解质是酸,其负极反应为:2H2-4e-═4H+,则正极反应为
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
;碱式氢氧燃料电池的电解质是碱,其正极反应表示为:O2+2H2O+4e-═4OH-,则负极反应为:2H2-4e-+4OH-=4H2O
2H2-4e-+4OH-=4H2O
.(3)蓄电池Pb+PbO2+2H2SO4
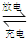 2PbSO4+2H2O放电时,正极电极反应式
2PbSO4+2H2O放电时,正极电极反应式PbO2+2e-+SO42-+4H+=PbSO4+2H2O
PbO2+2e-+SO42-+4H+=PbSO4+2H2O
,当电路中通过0.5mol电子时,消耗H2SO4的物质的量0.5mol
0.5mol
,负极增重24
24
g.按要求书写下列热化学方程式
(1)N2(g)和H2(g)反应生成1molNH3(g)放出46.1KJ热量
(2)航天领域使用氢氧燃烧电池有酸式和碱式两种,它们放电时的总反应可以表示为2H2+O2=2H2O,酸式氢氧燃烧电池的电解池是酸.其负极反应可以表示为2H2-4e-=4H+,则其正极反应可以表示为; ;碱式氢氧燃烧电池的电解质是碱,其正极反应可以表示为:O2+2H2O+4e-=4OH-,则其负极反应可以表示为: .
(3)用石墨作电极电解NaCl水溶液阳极的电极反应 ,阴极的电极反应
(4)在粗铜精炼的反应中 当阳极,发生 (填“氧化”或“还原”)反应,阳极的电极反应
(5)将H+、Cu2+、SO42-、Cl-五种离子组成电解质按要求进行电解:以碳棒为电极,使电解质质量减少,水量不变进行电解,应采用的电解质是 、 .
查看习题详情和答案>>
(1)N2(g)和H2(g)反应生成1molNH3(g)放出46.1KJ热量
(2)航天领域使用氢氧燃烧电池有酸式和碱式两种,它们放电时的总反应可以表示为2H2+O2=2H2O,酸式氢氧燃烧电池的电解池是酸.其负极反应可以表示为2H2-4e-=4H+,则其正极反应可以表示为;
(3)用石墨作电极电解NaCl水溶液阳极的电极反应
(4)在粗铜精炼的反应中
(5)将H+、Cu2+、SO42-、Cl-五种离子组成电解质按要求进行电解:以碳棒为电极,使电解质质量减少,水量不变进行电解,应采用的电解质是