网址:http://m.1010jiajiao.com/timu_id_1741300[举报]
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量.此方案测定的结果误差较大,主要原因是:
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量.

(1)按此方案,以下制取CO2和实验使用的仪器的连接次序是
(2)装置⑤的作用是:
[方案三]:测定样品与水充分反应后溶液的体积Vml,再从中取V1mL溶液,装入锥形瓶,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量.
(1)此方案中酸碱滴定时,选用的滴定管为
(2)若用甲基橙做指示剂,达到滴定终点时的现象为
为测定某含有杂质Na2O的Na2O2样品的纯度,3个小组分别设计如下方案。首先准确称量样品mg,然后,按照以下方案进行实验,请你完成相关内容:
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量。Na2O2跟水反应的离子方程式是: ;根据所给数据计算出的试样中Na2O2含量的代数式为 。
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。

(1)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是 。(填写仪器编号)
(2)装置①⑤的作用分别是:① ⑤ 。
[方案三]:测定样品与水充分反应后溶液的体积VmL。,再从中取V1mL溶液装入锥形瓶中,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量。
(1)方案中酸碱滴定时,选用的滴定管为右图中的 (填仪器编号)。
(2)若用酚酞做指示剂,达到滴定终点时的现象为 。
(3)三个方案相比测定结果最准确的是 。
查看习题详情和答案>>[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量。Na2O2跟水反应的离子方程式是: ;根据所给数据计算出的试样中Na2O2含量的代数式为 。
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。

(1)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是 。(填写仪器编号)
(2)装置①⑤的作用分别是:① ⑤ 。
[方案三]:测定样品与水充分反应后溶液的体积VmL。,再从中取V1mL溶液装入锥形瓶中,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量。
(1)方案中酸碱滴定时,选用的滴定管为右图中的 (填仪器编号)。
(2)若用酚酞做指示剂,达到滴定终点时的现象为 。

(3)三个方案相比测定结果最准确的是 。
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量.此方案测定的结果误差较大,主要原因是:______;
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量.
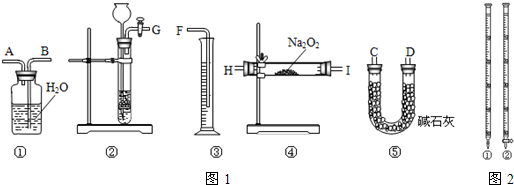
(1)按此方案,以下制取CO2和实验使用的仪器的连接次序是______.(填写如图1所示仪器编号)
(2)装置⑤的作用是:______.
[方案三]:测定样品与水充分反应后溶液的体积Vml,再从中取V1mL溶液,装入锥形瓶,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量.
(1)此方案中酸碱滴定时,选用的滴定管为______(填如图2所示仪器编号).
(2)若用甲基橙做指示剂,达到滴定终点时的现象为______.你认为方案二、方案三中测定结果比较准确的是______.
为测定某含有杂质Na2O的Na2O2样品的纯度,3个小组分别设计如下方案.首先准确称量样品mg,然后,按照以下方案进行实验:
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量.此方案测定的结果误差较大,主要原因是:________;
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量.

(1)按此方案,以下制取CO2和实验使用的仪器的连接次序是________.(填写仪器编号)
(2)装置⑤的作用是:________.
[方案三]:测定样品与水充分反应后溶液的体积V mL,再从中取V 1 mL溶液,装入锥形瓶,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量.
(1)此方案中酸碱滴定时,选用的滴定管为________(填仪器编号).
(2)若用甲基橙做指示剂,达到滴定终点时的现象为________.你认为方案二、方案三中测定结果比较准确的是________.