网址:http://m.1010jiajiao.com/timu_id_1739970[举报]
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么![]() (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量![]() m(H20),由此计算
m(H20),由此计算![]() 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):

请回答下列问题:[来源:学§科§网Z§X§X§K]
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大![]() 的是_______________ (填序号);
的是_______________ (填序号);
![]() Cu0未完全起反应 ② CuO不
Cu0未完全起反应 ② CuO不![]() 干燥
干燥
![]() Cu0中混有不反应的杂质 ④ 碱石灰不干燥
Cu0中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________![]() _____和_______________达到实验目的。
_____和_______________达到实验目的。
选考题(请考生在第18、19、20三题中任选一题做答,如果多做,则按所做的第一题计分。做答时用2B铅笔在答题卡上把所选题目的题号涂黑)。
第18、19、20三题的第Ⅰ题为选择题,在给出的四个选项中,至少有两项是符合
题目要求的,请将符合题目要求的选项标号填在答题卡相应位置;第Ⅱ题为非选择题,
请在答题卡相应位置做答并写明小题号。
查看习题详情和答案>>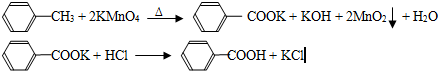
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为
(2)无色液体A是
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解, 冷却 冷却 过滤 过滤 |
得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中, 滴入适量的硝酸酸化的AgNO3溶液 滴入适量的硝酸酸化的AgNO3溶液 |
生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, 加热使其融化,测其熔点 加热使其融化,测其熔点 |
熔点为122.4℃ 熔点为122.4℃ |
白色晶体是苯甲酸 |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水.
(1)[提出假设]假设一:该漂白粉未变质,含
假设二:该漂白粉全部变质,含
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3.
(2)[进行实验]在答题卡上完成下表写实验步骤、预期现象与结论(不必检验Ca2+、Cl-):
| 实验步骤 | 预期现象和结论 | |
| 1 | 用试管取少量澄清石灰水备用,用另一试管取少量样品,再 向试管加入1mol/L的稀盐酸 向试管加入1mol/L的稀盐酸 |
若无气体放出且澄清石灰水未见浑浊,则假设一成立; |
| 2 | 取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水 取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水 |
品红不褪色,而石灰水变浑浊,假设二成立 品红不褪色,而石灰水变浑浊,假设二成立 |
| ③ | 取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水 取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水 |
品红溶液褪色,澄清石灰水变浑浊,假设三成立. 品红溶液褪色,澄清石灰水变浑浊,假设三成立. |
Ⅰ.小组成员认为黑色物质中含有氧化铜,是反应过程中生成的Cu(OH)2分解产生的.请说明反应过程中产生Cu(OH)2的原因
Ⅱ.兴趣小组对黑色粉末状物质的组成进行了实验探究.请完成下列实验报告.
限定实验仪器与试剂:1g 黑色粉末、试管、玻璃棒、药匙、滴管、酒精灯、试管夹、稀H2SO4、浓HNO3、稀NaOH溶液、蒸馏水.
实验报告
(1)实验课题:探究黑色粉末的组成
(2)设计实验方案(不要在答题卡上作答)
(3)实验过程
| 实验操作 | 预期现象与结论 |
限选实验仪器与试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、1mol?L-1硫酸、1mol?L-1硝酸、1mol?L-1盐酸、2mol?L-1NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
完成以下实验探究过程:
(1)提出假设:
根据题意,该白色粉末的组成有
(2)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要在答题卡上作答).
(3)根据②的实验方案,叙述实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论 |
| 步骤1: 用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管 用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管 |
白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl 白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl |
| 步骤2: 用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡 用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡 |
固体溶解得无色溶液 固体溶解得无色溶液 |
| 步骤3: 向试管B中滴加过量的Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置 向试管B中滴加过量的Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置 |
有白色沉淀生成,证明原白色粉末含有K2SO4 有白色沉淀生成,证明原白色粉末含有K2SO4 |
| 步骤4: 取试管B中上层清液少量于试管C中,滴加AgNO3溶液和1mol?L-1硝酸 取试管B中上层清液少量于试管C中,滴加AgNO3溶液和1mol?L-1硝酸 |
有白色沉淀生成,证明原白色粉末含有NaCl 有白色沉淀生成,证明原白色粉末含有NaCl |
| … | … … |