摘要:24.已知氯元素能形成三种相对分子质量分别为70.72.74的氯气的分子.若它们的分子数之比为a:b:c.则氯元素有 种稳定的同位素.它们在氯气中的原子数之比35Cl:37Cl为
网址:http://m.1010jiajiao.com/timu_id_1737791[举报]
已知氯元素能形成三种相对分子质量分别为70,72,74的氯气的分子,若它们的分子数之比为a:b:c,则氯元素有______种稳定的同位素,它们在氯气中的原子数之比35Cl:37Cl为___________________________(用a,b,c表示)
查看习题详情和答案>>已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)E的核外电子排布式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
查看习题详情和答案>>
(1)A、B、C的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(2)B的氢化物的分子空间构型是
三角锥型
三角锥型
.其中心原子采取sp3
sp3
杂化.(3)写出化合物AC2的电子式


N2O
N2O
.(4)E的核外电子排布式是
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
,ECl3形成的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3
[Cr(NH3)4(H2O)2]Cl3
.(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式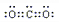
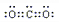 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)ECl3形成的配合物的化学式为
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
查看习题详情和答案>>
(1)A、B、C的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(2)B的氢化物的分子空间构型是
三角锥形
三角锥形
.其中心原子采取sp3
sp3
杂化.(3)写出化合物AC2的电子式
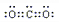
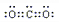
N2O
N2O
.(4)ECl3形成的配合物的化学式为
[Cr(NH3)4(H2O)2]Cl3
[Cr(NH3)4(H2O)2]Cl3
.(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
4Mg+10HNO3=4Mg(NO3)2+NH4NO3 +3H2O
4Mg+10HNO3=4Mg(NO3)2+NH4NO3 +3H2O
.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)E的核外电子排布式是
查看习题详情和答案>>
(1)A、B、C的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(2)B的氢化物的分子空间构型是
三角锥型
三角锥型
.其中心原子采取sp3
sp3
杂化.(3)写出化合物AC2的电子式


N2O
N2O
.(4)E的核外电子排布式是
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
,ECl3形成的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3
[Cr(NH3)4(H2O)2]Cl3
.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(2)写出化合物AC2的电子式 。AC2是由 键组成的 (填“极性”或“非极性”)分子。
(3)E的外围电子排布式是 ,在形成化合物时它的最高化合价为 , ECl3形成的配合物的化学式为 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
查看习题详情和答案>>