摘要:18.(2)3 NF3 + 5 H2O =2 NO + HNO3 + 9 HF 1:2
网址:http://m.1010jiajiao.com/timu_id_173761[举报]
已知元素A、B、C、D、E的原子序数依次递增.A与D相邻,D元素的M层电子数是其K层电子数的2倍,C元素的最外层电子数是其电子层数的3倍,E的原子序数为29.请回答下列问题:
(1)下列有关说法正确的是
①D的单质常可制取光导纤维;
②DC2属于分子晶体;
③第一电离能:B>A>D
④基态E2+的核外电子排布式为:1s22s22p63s23p63d9
⑤BH3分子的空间构型为三角锥形
(2)与B2互为等电子体的分子为 ;
(3)A与氢原子形成的相对分子质量为28的化合物分子,A采取 杂化,且一个分子中有 个σ键;
(4)A、B两种元素形成的氢化物中,沸点较高的是 (填物质名称),其主要原因是 ;
(5)向含E2+的溶液中逐滴加入过量氨水时,可观察到 .
查看习题详情和答案>>
(1)下列有关说法正确的是
①D的单质常可制取光导纤维;
②DC2属于分子晶体;
③第一电离能:B>A>D
④基态E2+的核外电子排布式为:1s22s22p63s23p63d9
⑤BH3分子的空间构型为三角锥形
(2)与B2互为等电子体的分子为
(3)A与氢原子形成的相对分子质量为28的化合物分子,A采取
(4)A、B两种元素形成的氢化物中,沸点较高的是
(5)向含E2+的溶液中逐滴加入过量氨水时,可观察到
(Ⅰ)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大.W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物.
(1)W位于元素周期表第
W的气态氢化物稳定性比H2O(g)
(2)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
(3)Fe(s)+
O2(g)=FeO(s)△H+-272.0KJ?mol-1
2X(s)+
O2(g)=x2o3(s)△H=-1675.7KJ?mol-1
X的单质和FeO反应的热化学方程式是
(Ⅱ)已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为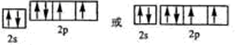
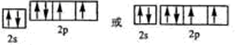 _
_
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
查看习题详情和答案>>
(1)W位于元素周期表第
二
二
周期第ⅤA
ⅤA
族.W的气态氢化物稳定性比H2O(g)
弱
弱
(填“强”或“弱”).(2)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
2H2SO4(浓)+Cu
CuSO4+SO2↑+2H2O
| ||
2H2SO4(浓)+Cu
CuSO4+SO2↑+2H2O
.
| ||
(3)Fe(s)+
| 1 |
| 2 |
2X(s)+
| 3 |
| 2 |
X的单质和FeO反应的热化学方程式是
Al(S)+FeO(S)+
O2 (g)=
Al2O3(S)+Fe(S)△H=-565.85KJ/mol
| 1 |
| 4 |
| 1 |
| 2 |
Al(S)+FeO(S)+
O2 (g)=
Al2O3(S)+Fe(S)△H=-565.85KJ/mol
.| 1 |
| 4 |
| 1 |
| 2 |
(Ⅱ)已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
(1)X元素原子基态时的电子排布式为
1s22s22p63s23p63d104s24p3
1s22s22p63s23p63d104s24p3
(2)Y元素原子的价层电子的轨道表示式为
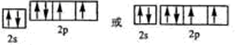
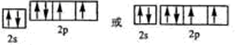
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
三角锥形
三角锥形
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O
As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O
. 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.| a | b | ||||||||||||||||
| c | d | e | |||||||||||||||
| f | g | ||||||||||||||||
(1)a的氢化物的分子构型为
三角锥形
三角锥形
,中心原子的杂化形式为sp3
sp3
;d在空气中燃烧产物的分子构型为V形
V形
,中心原子的杂化形式为sp2
sp2
,该分子是极性
极性
(填“极性”或“非极性”)分子.(2)b、d、e三种元素的氢化物中的沸点最高的是
HF
HF
,原因是:HF分子间形成氢键,HCl、H2S分子间没有氢键
HF分子间形成氢键,HCl、H2S分子间没有氢键
.(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.此配合离子空间构型为
平面正方形
平面正方形
,请写出生成此配合离子的离子方程式:Cu2++4H2O=[Cu(H2O)4]2+
Cu2++4H2O=[Cu(H2O)4]2+
.(4)f(NH3)5BrSO4可形成两种配合物,已知f3+的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2 溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为
[Co(NH3)5SO4]Br
[Co(NH3)5SO4]Br
,该配合物的配体是NH3
NH3
、SO42-
SO42-
;(5)c单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
c单质晶体中原子的配位数为
12
12
.若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M.该晶体的密度为| M | ||
4
|
| M | ||
4
|
请回答下列问题:
(1)①[Cu(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素(核电荷数24),该元素基态原子的电子排布式是
(3)利用CO可以合成化工原料COCl2,则COCl2分子内含有
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键
(4)按要求写出第二周期非金属元素组成的中性分子的化学式及中心原子的杂化方式.三角锥形分子:分子式
(5)用价层电子对互斥理论推断第ⅣA族元素Sn形成的SnBr2分子中Sn-Br的键角
(6)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
查看习题详情和答案>>
(1)①[Cu(NH3)4]2+中存在的化学键类型有
AC
AC
(填序号).A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
平面正方型
平面正方型
.(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素(核电荷数24),该元素基态原子的电子排布式是
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
,与它同周期的基态原子中最外层电子数与铬相同的元素有Cu、K
Cu、K
(填元素符号).(3)利用CO可以合成化工原料COCl2,则COCl2分子内含有
D
D
(填标号).A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键
(4)按要求写出第二周期非金属元素组成的中性分子的化学式及中心原子的杂化方式.三角锥形分子:分子式
NF3
NF3
,杂化方式是sp3
sp3
;(5)用价层电子对互斥理论推断第ⅣA族元素Sn形成的SnBr2分子中Sn-Br的键角
<
<
120°(填“>”“<”或“=”).(6)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
C>H>Si
C>H>Si
.在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示.极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量.分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即=d?q,在非极性分子中因正负电荷重心重合,故μ为0.试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的有
(2)实验测得:μPF3=1.03、μBCl3=0.
①由此可知,PF3分子的空间构型为
②BC13分子的空间构型为
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上.已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0.试画出两种异构体的构型图,并比较在水中的溶解度.构型图:淡黄色者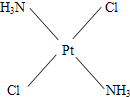
 ,棕黄色者
,棕黄色者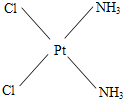
 ;在水中溶解度较大的是
;在水中溶解度较大的是
查看习题详情和答案>>
(1)HCl、CS2、H2S、SO2四种分子中μ=0的有
CS2
CS2
;(2)实验测得:μPF3=1.03、μBCl3=0.
①由此可知,PF3分子的空间构型为
三角锥形
三角锥形
;②BC13分子的空间构型为
平面正三角形
平面正三角形
,中心原子的杂化方式为sp2
sp2
.(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上.已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0.试画出两种异构体的构型图,并比较在水中的溶解度.构型图:淡黄色者




棕黄色者
棕黄色者
.