网址:http://m.1010jiajiao.com/timu_id_1737188[举报]
为测定某固体物质中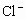 的质量分数,现用0.2mol/L的
的质量分数,现用0.2mol/L的 溶液滴定含1g样品的溶液(使样品中的氯化物与
溶液滴定含1g样品的溶液(使样品中的氯化物与 恰好完全反应),消耗
恰好完全反应),消耗 的质量分数是________.如果为了省去计算过程,当称取的样品的质量为某一数值时,可使滴定所用的
的质量分数是________.如果为了省去计算过程,当称取的样品的质量为某一数值时,可使滴定所用的 溶液的毫升数恰好等于样品中
溶液的毫升数恰好等于样品中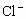 的质量分数a%中的a,那么应称取的样品的质量为________g.
的质量分数a%中的a,那么应称取的样品的质量为________g.
为测定某固体物质中Cl-的质量分数,现在用0.2 mol·L-1AgNO3溶液滴定含1 g样品的溶液(使样品中的氯化物与AgNO3恰好完全反应).
(1)若消耗AgNO3溶液V mL,则样品中Cl-的质量分数是多少?
(2)如果为了省去计算过程,当称取的样品的质量为某一数值时,可使滴定中所消耗的AgNO3溶液的毫升数恰好等于样品中Cl-的质量分数a%中的a,那么应称取的样品的质量为多少?
坩埚质量:15.286 1 g
第一次灼烧后坩埚和固体质量:15.620 9 g
第二次灼烧后坩埚和固体质量:15.620 5 g
第三次灼烧后坩埚和固体质量:15.620 5 g
则铁矿石中铁元素的质量分数为
A.63.2% B.90.3% C.6.32% D.34.4%
查看习题详情和答案>>为测定某Fe2O3和FeO混合物中Fe2O3的含量,往一定量样品中加入200 mL 5.0 mol·L-1硫酸,充分反应后,测得溶液中c(H+)=1.0 mol·L-1(设溶液体积仍为200 mL),再加入适量2.0 mol·L-1 NaOH溶液,使Fe2+、Fe3+完全沉淀,待沉淀全部变为红褐色后,过滤,洗涤、灼烧沉淀物,称得固体质量比原样品增加2.4 g.
(1)与样品发生反应的硫酸的物质的量为多少?
(2)需加入多少毫升NaOH溶液,才能使Fe3+、Fe2+恰好沉淀完全?
(3)该混合物中Fe2O3的质量分数是多少?
|
为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案: 方案一:铜铝混合物 方案二:铜铝混合物 下列有关判断中不正确的是 | |
| [ ] | |
A. |
溶液A和溶液B均可以是盐酸或NaOH溶液 |
B. |
若溶液B选用浓硝酸,测得铜的质量分数偏小 |
C. |
溶液A和溶液B选用稀硝酸 |
D. |
实验室中方案Ⅱ更便于实施 |