摘要:25.某同学设计了图3-5所示装置进行探究. (1)进行“铜和稀硝酸反应制取NO 的实验. ①制取NO的化学方程式: . ②收集气体前必须先 .然后才开始收集气体. (2)利用该装置制取并收集少量其他气体.请完成下表: 制取气体 药品 O2 . H2 溶液.Al (3)利用该装置进行实验.并根据产生氢气的量来确定某酸的结构: ①反应前.先对量气管进行第一次读数.读数时.应注意的操作是 .并使视线凹液面最低处相平,反应后.待 时.再对量气管进行第二次读数. ②实验数据记录如下:(表中读数已折合成标准状况下的数值) 编号 酸的质量 金属锌的质量 量气管第一次读数 量气管第二次读数 1 1.459 10.09 40ml. 264mL 2 1.459 10.09 30mi. 228mL 3 1.459 10.09 20mL 243mL 已知该酸的相对分子质量为145.根据上述数据可确定该酸是 元酸, ③如果第二次对量气管读数时仰视.则所测得的气体体积会 (填“偏大 .“偏小 或“不能确定 )
网址:http://m.1010jiajiao.com/timu_id_1734336[举报]
某同学设计了图3-5所示装置进行探究。(夹持装置已略去)
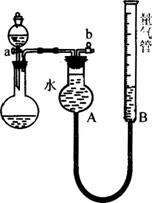
图3-5
(1)进行“铜和稀硝酸反应制取NO”的实验。
①制取NO的化学方程式:__________________________________________________。
②收集气体前必须先____________,然后才开始收集气体。
(2)利用该装置制取并收集少量其他气体,请完成下表:
制取气体 | 药品 |
O2 | _________、___________ |
H2 | __________溶液、Al |
(3)利用该装置进行实验,并根据产生氢气的量来确定某酸的结构:①反应前,先对量气管进行第一次读数。读数时,应注意的操作是____________,并使视线与凹液面最低处相平;反应后,待____________时,再对量气管进行第二次读数。
②实验数据记录如下:(表中读数已折合成标准状况下的数值)
编号 | 酸的质量 | 金属锌的质量 | 量气管第一次读数 | 量气管第二次读数 |
1 | 10. | 40mL | 264mL | |
2 | 1. | 10. | 30mL | 228mL |
3 | 1. | 10. | 20mL | 243mL |
已知该酸的相对分子质量为145。根据上述数据可确定该酸是___________元酸;
③如果第二次对量气管读数时仰视,则所测得的气体体积会___________(填“偏大”、“偏小”或“不能确定”)
查看习题详情和答案>>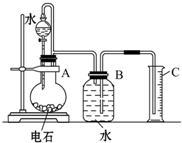 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.(1)烧瓶中发生反应的化学方程式为
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
.装置B、C的作用是装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
.(2)分液漏斗与烧瓶间用乳胶管连接的目的是
便于液体顺利滴下
便于液体顺利滴下
.(3)所用电石质量不能太大,否则
生成C2H2太多超过B的空间
生成C2H2太多超过B的空间
;也不能太小,否则无法测定其体积测定误差会更大
无法测定其体积测定误差会更大
;若容器B的容积为250mL,则所用电石的质量应在0.60
0.60
g左右(从后面数据中选填:0.03、0.60、1.00、1.50、2.00).(4)为了得到比较平稳的乙炔气流,实验室通常用
饱和食盐水
饱和食盐水
代替水进行实验.(5)实验中测得排入量筒中水的体积为VL、电石的质量为Wg.则电石中碳化钙的质量分数是
| 0.29V |
| W |
| 0.29V |
| W |
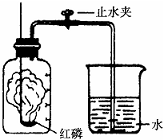 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹
夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是
充分反应掉集气瓶中的氧气
充分反应掉集气瓶中的氧气
.其反应的文字表达式为
红磷+氧气
五氧化二磷
| 点燃 |
红磷+氧气
五氧化二磷
;步骤③中打开止水夹后观察到的现象是| 点燃 |
水沿导管倒流进入集气瓶中,倒流至集气瓶容积的
处
| 1 |
| 5 |
水沿导管倒流进入集气瓶中,倒流至集气瓶容积的
处
,由此可得出空气中氧气的体积分数约为| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
(2)该实验可推论出氮气
难
难
(填“易”或“难”)溶于水和其化学性质不活泼
不活泼
(填“活泼”或“不活泼”)的结论.(3)若将红磷换成炭粉,该实验能否获得成功?为什么?
不能成功,木炭和氧气反应又生成二氧化碳,没有改变集气瓶内的压强
不能成功,木炭和氧气反应又生成二氧化碳,没有改变集气瓶内的压强
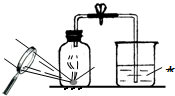
(4)某同学对实验进行反思后,提出了改进方法(如图所示 ),你认为改进后的优点是:
环保、误差小
环保、误差小
.
(4)图是测定空气中中氧气含量的实验.在实验过程中,观察到红磷燃烧的现象是:剧烈燃烧、放出大量热和
产生大量白烟
产生大量白烟
.排除了气密性不好等因素外,过量红磷燃烧熄灭后集气瓶内仍有
仍有
(填”“仍有”或“没有”)残余的氧气. 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹
夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是______.
其反应的文字表达式为______;步骤③中打开止水夹后观察到的现象是______,由此可得出空气中氧气的体积分数约为______.
(2)该实验可推论出氮气______(填“易”或“难”)溶于水和其化学性质______(填“活泼”或“不活泼”)的结论.
(3)若将红磷换成炭粉,该实验能否获得成功?为什么?______
(4)某同学对实验进行反思后,提出了改进方法(如图所示 ),你认为改进后的优点是:______.
(4)图是测定空气中中氧气含量的实验.在实验过程中,观察到红磷燃烧的现象是:剧烈燃烧、放出大量热和______.排除了气密性不好等因素外,过量红磷燃烧熄灭后集气瓶内______(填”“仍有”或“没有”)残余的氧气.
查看习题详情和答案>>
(10分)某同学设计了如图所示的装置(夹持装置已略去)来探究影响化学反应速率的因素。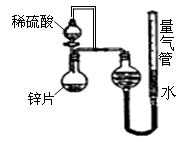
(1)圆底烧瓶中发生反应的离子方程式是
__________________________________________
(2)用上述装置进行实验,以生成15.0mL气体为计时终点,
结果为t1﹥t2
| 序号 | Ⅴ(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
| Ⅰ | 10 | 1 | t1 |
| Ⅱ | 10 | 3 | t2 |
比较实验Ⅰ和实验Ⅱ可以得出的结论是__________________________________________
(3)实验中向烧瓶中滴入的稀硫酸的体积(其他操作都正确),对测定气体体积的影响_____ __________ (填“偏大”、“偏小”、“无影响”)
(4)将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含的杂质可能是(填序号)________
a.石墨 b.银 c.铜 d.沙粒(二氧化硅)
(5)要加快该反应的反应速率,还可以采取的措施有________________________(任填一种即可) 查看习题详情和答案>>