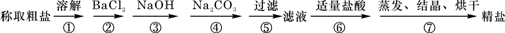题目内容
某同学设计了图3-5所示装置进行探究。(夹持装置已略去)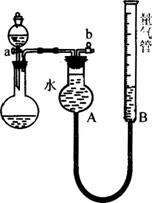
图3-5
(1)进行“铜和稀硝酸反应制取NO”的实验。
①制取NO的化学方程式:__________________________________________________。
②收集气体前必须先____________,然后才开始收集气体。
(2)利用该装置制取并收集少量其他气体,请完成下表:
制取气体 | 药品 |
O2 | _________、___________ |
H2 | __________溶液、Al |
(3)利用该装置进行实验,并根据产生氢气的量来确定某酸的结构:①反应前,先对量气管进行第一次读数。读数时,应注意的操作是____________,并使视线与凹液面最低处相平;反应后,待____________时,再对量气管进行第二次读数。
②实验数据记录如下:(表中读数已折合成标准状况下的数值)
编号 | 酸的质量 | 金属锌的质量 | 量气管第一次读数 | 量气管第二次读数 |
1 | 10. | 40mL | 264mL | |
2 | 1. | 10. | 30mL | 228mL |
3 | 1. | 10. | 20mL | 243mL |
已知该酸的相对分子质量为145。根据上述数据可确定该酸是___________元酸;
③如果第二次对量气管读数时仰视,则所测得的气体体积会___________(填“偏大”、“偏小”或“不能确定”)
(1)①3Cu+8HNO3 (稀)=3Cu(NO3)2+2NO↑+4H2O ②排除装置中的空气
(2)H2O2 MnO2 NaOH
(3)①使A、B两管液面保持在同一平面上 液面保持不变 ②二 ③偏小

练习册系列答案
相关题目
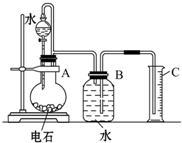 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
 在两个体积均为1L的恒容容器a和b中模拟一碳化学合成甲醛,合成过程中的原理可表示为CO(g)+H2(g)?HCHO(g),其中容器a中使用催化剂.两容器中CO和H2的物质的量相同,均为1mol.试回答下列问题:
在两个体积均为1L的恒容容器a和b中模拟一碳化学合成甲醛,合成过程中的原理可表示为CO(g)+H2(g)?HCHO(g),其中容器a中使用催化剂.两容器中CO和H2的物质的量相同,均为1mol.试回答下列问题: 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):