摘要:18.某校化学兴趣小组设计以下装置进行不同的实验其中a为用于鼓人空气的气囊.b为螺旋状铜丝.C为NaOH溶液.d为冰水混合物. Ⅰ.制取并收集乙烯气体:该反应的化学方程式是 .实验过程中发现反应混合物变黑.据此推测生成的乙烯中可能含有的具有刺激性气味的气体杂质是 .该实验选用的装置是 . Ⅱ.乙酸乙酯的制取:.该反应的化学方程式是 ,该实验选用的装置有 .实验开始时.向反应装置中添加试剂的顺序为 .向接收装置中加入的试剂是 ,实验过程中.为加快酯化反应的速率.通常采用的措施是 ,实验结束时.为得到乙酸乙酯而进行的分离操作是 . Ⅲ. 乙醇的催化氧化实验:反应的化学方程式是 . 选用的装置是 .
网址:http://m.1010jiajiao.com/timu_id_1734061[举报]
某校化学兴趣小组设计以下装置进行不同的实验其中a为用于鼓入空气的气囊,b为螺旋状铜丝,C为NaOH溶液,d为冰水混合物。

Ⅰ.制取并收集乙烯气体:该反应的化学方程式是 ,实验过程中发现反应混合物变黑,据此推测生成的乙烯中可能含有的具有刺激性气味的气体杂质是 ,该实验选用的装置是 (填装置编号)。
Ⅱ.乙酸乙酯的制取:、该反应的化学方程式是 ;该实验选用的装置有 (填装置编号)。实验开始时,向反应装置中添加试剂的顺序为 ,向接收装置中加入的试剂是 ;实验过程中,为加快酯化反应的速率,通常采用的措施是 ;实验结束时,为得到乙酸乙酯而进行的分离操作是 (写出操作名称)。
Ⅲ. 乙醇的催化氧化实验:反应的化学方程式是 , 选用的装置是 (填装置编号)。
查看习题详情和答案>>某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验.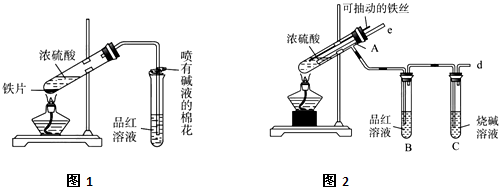
(1)比较两个实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO2防止其污染环境;
②
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到”液封”作用阻止SO2气体逸出而防止污染环境;二是
(3)能说明有SO2气体产生的实验现象是
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;
Ⅱ:只含有Fe2+;
Ⅲ:既有Fe3+又有Fe2+.
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀硫酸 C.KSCN溶液 D.酸性KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液 G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的
验证Ⅲ:步骤1.取试样,滴加少量的
步骤2.再取适量的试样滴加少量的
查看习题详情和答案>>

(1)比较两个实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO2防止其污染环境;
②
便于控制反应的发生和停止
便于控制反应的发生和停止
.(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到”液封”作用阻止SO2气体逸出而防止污染环境;二是
停止加热时,能防止倒吸或平衡压强
停止加热时,能防止倒吸或平衡压强
.(3)能说明有SO2气体产生的实验现象是
品红溶液褪色
品红溶液褪色
.(4)反应一段时间后,用滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;
Ⅱ:只含有Fe2+;
Ⅲ:既有Fe3+又有Fe2+.
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀硫酸 C.KSCN溶液 D.酸性KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液 G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的
C
C
(填试剂序号,下同),振荡,再滴加少量的G
G
,根据溶液颜色的变化可确定假设Ⅱ是否正确.验证Ⅲ:步骤1.取试样,滴加少量的
C(或F)
C(或F)
(填试剂序号),溶液的颜色变红(或蓝)
红(或蓝)
色,则试样中含有Fe3+发生反应的离子方程式为Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+
Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+
.步骤2.再取适量的试样滴加少量的
D
D
(填试剂序号),溶液颜色的变化为酸性KMnO4溶液的浅红色褪去
酸性KMnO4溶液的浅红色褪去
,则试样中含有Fe2+. 某校化学兴趣小组在实验里制取乙烯时,加热时,因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气和炭黑.
某校化学兴趣小组在实验里制取乙烯时,加热时,因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气和炭黑.(1)写出该副反应的化学方程式
CH3CH2OH+4H2SO4(浓)
4SO2↑+CO2↑+7H2O+C
| ||
CH3CH2OH+4H2SO4(浓)
4SO2↑+CO2↑+7H2O+C
.
| ||
(2)用编号为A~B的实验装置设计一个实验,以验证上述反应混合气体中含CO2、SO2和水蒸气.请从图中选用所需的仪器(可重复选用)组成一套进行检验反应产物的装置.现提供浓H2SO4、乙醇和酸性KMnO4溶液,其它试剂自选.(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用(可以不填满).
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| C | 浓H2SO4和乙醇 | 反应器(或发生气体) |
B B |
无水CuSO4 无水CuSO4 |
检验H2O 检验H2O |
A A |
品红溶液 品红溶液 |
检验SO2 检验SO2 |
A A |
酸性KMnO4溶液 酸性KMnO4溶液 |
吸收余下的SO2 吸收余下的SO2 |
A A |
澄清石灰水 澄清石灰水 |
检验CO2的存在 检验CO2的存在 |
某校化学兴趣小组的同学利用漂白粉与稀硫酸在加热条件下反应制取Cl2,其反应的化学方程式为:Ca(ClO)2+CaCl2+2H2SO4
2CaSO4+2Cl2↑+2H2O.以下是制取Cl2并验证其部分性质的实验装置.

试回答下列问题:
(1)请在上图(右上装置中)选择满足实线框图I的气体发生装置:
(2)实验装置Ⅲ的作用是
(3)一段时间后,装置Ⅲ的溶液仍呈强碱性,其中肯定存在Cl-、OH-和SO42-,请设计实验探究该吸收液中可能存在的其它阴离子(不考虑空气中CO2的影响).
①提出合理假设:假设1:只存在SO32-; 假设2:只存在ClO-; 假设3:
②设计实验方案进行实验,请写出实验步骤以及预期现象和结论.实验试剂:3mol?L-1 H2SO4、1mol?L-1 NaOH、0.01mol?L-1 KMnO4、淀粉KI溶液、紫色石蕊试液.
查看习题详情和答案>>
| ||

试回答下列问题:
(1)请在上图(右上装置中)选择满足实线框图I的气体发生装置:
b
b
(填代号);(2)实验装置Ⅲ的作用是
吸收多余氯气,防止污染大气
吸收多余氯气,防止污染大气
;(3)一段时间后,装置Ⅲ的溶液仍呈强碱性,其中肯定存在Cl-、OH-和SO42-,请设计实验探究该吸收液中可能存在的其它阴离子(不考虑空气中CO2的影响).
①提出合理假设:假设1:只存在SO32-; 假设2:只存在ClO-; 假设3:
既不存在SO32-也不存在ClO-
既不存在SO32-也不存在ClO-
②设计实验方案进行实验,请写出实验步骤以及预期现象和结论.实验试剂:3mol?L-1 H2SO4、1mol?L-1 NaOH、0.01mol?L-1 KMnO4、淀粉KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol?L-1 H2SO4至溶液显酸性,然后将所得溶液分置于A、B试管中. | / |
| 步骤2: | |
| 步骤3: |
某校化学兴趣小组在探究铁与浓硫酸的反应时,将教材中铜与浓硫酸反应的实验装置(图Ⅰ)改为图Ⅱ所示的装置.
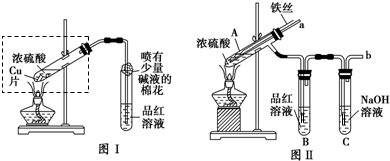
请回答下列问题:
(1)写出图Ⅰ中虚框处发生反应的化学方程式 .
(2)图Ⅱ实验装置与图Ⅰ相比较,其优点是:①能更好地吸收有毒气体SO2,防止其污染环境;② .
(3)下列对导管a的作用分析中正确的是 (填字母).
A.加热反应过程中,可上下移动导管a,起搅拌作用
B.停止加热,试管内的压强减小,从导管a进入的空气可增大试管A内的压强,防止倒吸
C.停止反应,撤装置之前往导管a中通入空气,可排除装置内的SO2气体,防止其污染环境
(4)反应一段时间后,将试管A取下,然后将试管A中溶液倒入另一盛有适量水的试管D中.该小组同学为确定溶液中所存在的金属离子,进行下列探究过程.
①提出假设:
假设Ⅰ:只含有Fe3+.假设Ⅱ: .假设Ⅲ: .
②实验设计:
分别取少量试管D中溶液,选用提供的试剂,设计简单的实验检验溶液中所存在的金属离子.请填写下表空白(可以不填满,也可以增加).
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液.
查看习题详情和答案>>

请回答下列问题:
(1)写出图Ⅰ中虚框处发生反应的化学方程式
(2)图Ⅱ实验装置与图Ⅰ相比较,其优点是:①能更好地吸收有毒气体SO2,防止其污染环境;②
(3)下列对导管a的作用分析中正确的是
A.加热反应过程中,可上下移动导管a,起搅拌作用
B.停止加热,试管内的压强减小,从导管a进入的空气可增大试管A内的压强,防止倒吸
C.停止反应,撤装置之前往导管a中通入空气,可排除装置内的SO2气体,防止其污染环境
(4)反应一段时间后,将试管A取下,然后将试管A中溶液倒入另一盛有适量水的试管D中.该小组同学为确定溶液中所存在的金属离子,进行下列探究过程.
①提出假设:
假设Ⅰ:只含有Fe3+.假设Ⅱ:
②实验设计:
分别取少量试管D中溶液,选用提供的试剂,设计简单的实验检验溶液中所存在的金属离子.请填写下表空白(可以不填满,也可以增加).
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液.
| 步骤 | 所选试剂 | 现象及结论 |
| 1 | ||
| 2 | ||
| 3 |