网址:http://m.1010jiajiao.com/timu_id_1733553[举报]
请你与某小组的同学共同进行乙醇与乙酸酯化反应的探究实验:
⑴要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是: 。
⑵下边是实验室制取乙酸乙酯的装置图,其中小试管中装入的物质是 。
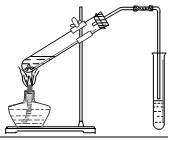
⑶分离小试管中制取的乙酸乙酯应使用的仪器叫做 ;分离时,乙酸乙酯应该从仪器
(填:“下口放” 或“上口倒”) 出。
⑷实验完毕,发现大试管中的反应液有些变黑,其原因是 。
⑸他们反复实验,得出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | X |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
表中数据X的范围是 ;实验①与实验⑤探究的目的是 ;
若乙醇价格为500元/kmol,乙酸价格为800元/kmol,乙酸乙酯价格为1600元/kmol,结合表中实验②③④的数据,你能得出的结论是 。
查看习题详情和答案>>乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体。某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答。
【观察与思考】
⑴ 乙醇分子的核磁共振氢谱有 个吸收峰。
【活动与探究】
⑵ 甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
| ② | ||
⑶ 乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次。则此时乙醇发生反应的化学方程式为 。
 欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为 。
欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为 。
【交流与讨论】
⑷ 丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边
慢慢加入2 mL浓硫酸和2 mL冰醋酸,按右图所示连接
好装置,请指出该装置的主要错误是 。
假如乙醇分子中的氧原子为18O原子,则发生此反应后
1 8O原子将出现在生成物 中(填字母)。
A.水 B.乙酸乙酯 C.水和乙酸乙酯
查看习题详情和答案>>乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
[观察与思考]
(1)乙醇分子的核磁共振氢谱有________个吸收峰.
[活动与探究]
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满).

(3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次.则此时乙醇发生反应的化学方程式为________.欲验证此实验的有机产物,可以将产物加入盛有________的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为________.
[交流与讨论]
(4)丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL浓硫酸和2 mL冰醋酸,按下图所示连接好装置,请指出该装置的主要错误是________.假如乙醇分子中的氧原子为18O原子,则发生此反应后1 8O原子将出现在生成物________中(填字母).

A、水
B、乙酸乙酯
C、水和乙酸乙酯
某研究性学习小组为确定某蜡状有机物
A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究.请你参与过程探究.1.实验式的确定
(1)取样品A进行燃烧法测定.发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和0.15 mol H2O.据此得出的结论是________.
(2)另一实验中,取3.4 g蜡状有机物A在3.36 L(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成2.8 L CO2和液态水.
由此得出的实验式是________.
2.结构式的确定(经测定A的相对分子质量为136)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有________.
(4)进行核磁共振,发现只有两个特征峰,且面积比为2∶1,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收.图谱如下:

则
A的结构简式为________.(本题共16分)某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案: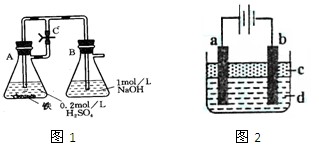
[实验设计]
方法一:按照图1进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行。最终在_______容器中观察到白色沉淀,该实验中涉及到的化学方程式有: 。
方法二:按图2进行实验,最终在两极间的溶液中首先观察到白色沉淀。请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl2溶液 ⑥乙醇 ⑦Fe棒 ⑧植物油 ⑨碳棒
a为___________,b为___________,c为___________,d为___________。(填序号)
[探究思考]实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3。这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+。 |
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2·nH2O所致。用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势。
加热时,“方法一”中弹簧夹C应处于___________(填“打开”或“关闭”)状态,容器A中的反应须处于___________(填“停止”或“发生”)状态。写出该实验中支持乙同学观点的化学方程式_______________。
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路。 。 查看习题详情和答案>>