题目内容
请你与某小组的同学共同进行乙醇与乙酸酯化反应的探究实验:
⑴要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是: 。
⑵下边是实验室制取乙酸乙酯的装置图,其中小试管中装入的物质是 。
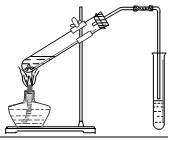
⑶分离小试管中制取的乙酸乙酯应使用的仪器叫做 ;分离时,乙酸乙酯应该从仪器
(填:“下口放” 或“上口倒”) 出。
⑷实验完毕,发现大试管中的反应液有些变黑,其原因是 。
⑸他们反复实验,得出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | X |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
表中数据X的范围是 ;实验①与实验⑤探究的目的是 ;
若乙醇价格为500元/kmol,乙酸价格为800元/kmol,乙酸乙酯价格为1600元/kmol,结合表中实验②③④的数据,你能得出的结论是 。
⑴先向大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸
⑵饱和碳酸钠溶液
⑶分液漏斗 上口倒
⑷热浓硫酸将反应剩余的乙醇和乙酸炭化
⑸1.57~1.76;探究增加乙酸的反应量对乙酸乙酯产量的影响;由于存在化学平衡,即使不断地增加廉价原料,产物的量增加也越来越少。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
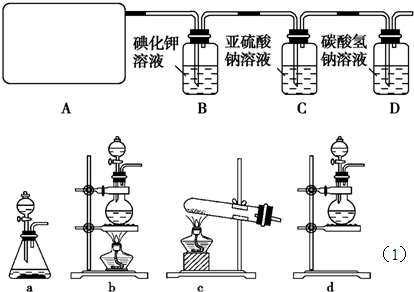
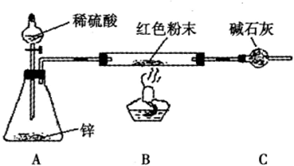

 如下的问题,探究。请你协助该小组的同学完成下列研究。
如下的问题,探究。请你协助该小组的同学完成下列研究。
 能被NH3还原吗?
能被NH3还原吗? 红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质
红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质 是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。
是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。