网址:http://m.1010jiajiao.com/timu_id_1732785[举报]
(6分)中学化学常见的物质A、B、C、D、E、X有如图所示转化关系。已知A、D是单质,B为氧化物,反应①在高温下发生。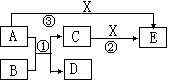
(1)若A、D、X为非金属单质,E是常见的温室气体,则A为____________,X为___________(用化学式填空)。
(2)若A为金属单质,D为非金属单质,X为盐酸,则反应①的化学方程式为________________;反应②的离子方程式________________________________。
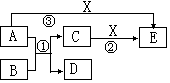
(1)若A、D、X为非金属单质,E是常见的温室气体,则A为____________,X为___________(用化学式填空)。
(2)若A为金属单质,D为非金属单质,X为盐酸,则反应①的化学方程式为________________;反应②的离子方程式________________________________。
物质A、B、C、D、E、F、G、H、I、J有如图所示的转化关系。

图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素。其它信息见下表:
|
编号 |
信 息 |
|
1 |
D为地壳中含量最高的元素组成的单质 |
|
2 |
E为酸性气态氧化物 |
|
3 |
F的浓溶液常做干燥剂 |
|
4 |
H为淡黄色固体化合物 |
|
5 |
电解饱和J溶液是工业重要反应 |
|
6 |
C为离子化合物,阴、阳离子均含有金属元素 |
(1)写出G的化学式: ,指出H中化学键的类型: 。
(2)常温下测得一定浓度的C溶液的pH=10,用离子方程式表示其原因 。
(3)写出与H相对分子质量相同,且它们的阴离子所含的电子数、电荷数也均相同的化合物的化学式 。
(4)写出C溶液中通入过量CO2的化学方程式: 。

(5)通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中三种含Y元素的离子,其中两种离子物质的量(n)与反应时间(t)的变化示意图如上图所示,写出该反应的离子方程式是 ,该苛性钾溶液中KOH的质量是 g。
查看习题详情和答案>>

图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素。其它信息见下表:
| 编号 | 信 息 |
| 1 | D为地壳中含量最高的元素组成的单质 |
| 2 | E为酸性气态氧化物 |
| 3 | F的浓溶液常做干燥剂 |
| 4 | H为淡黄色固体化合物 |
| 5 | 电解饱和J溶液是工业重要反应 |
| 6 | C为离子化合物,阴、阳离子均含有金属元素 |
(1)写出G的化学式: ,指出H中化学键的类型: 。
(2)常温下测得一定浓度的C溶液的pH=10,用离子方程式表示其原因 。
(3)写出与H相对分子质量相同,且它们的阴离子所含的电子数、电荷数也均相同的化合物的化学式 。
(4)写出C溶液中通入过量CO2的化学方程式: 。

(5)通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中三种含Y元素的离子,其中两种离子物质的量(n)与反应时间(t)的变化示意图如上图所示,写出该反应的离子方程式是 ,该苛性钾溶液中KOH的质量是 g。
Ⅰ.原子半径:A<C<B<E<D
Ⅱ.原子的最外层电子数:A=D C=E A+B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式


(2)写出某黑色含F的磁性氧化物在E的最高价氧化物对应水化物的稀溶液中反应的离子方程式:
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目:


(5)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2.则该复盐的化学式为