网址:http://m.1010jiajiao.com/timu_id_1731961[举报]
(15分)A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分产物省略)。请按要求回答下列问题:

(1) 若A是氯碱工业的一种重要产品,通常状况下D是一种非极性气体分子,则D的结构式为 ,A与D以物质的量3:2反应后的溶液中离子浓度的大小顺序为:
(2) 若D为某金属单质,向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为 ;将B的溶液加热蒸干再灼烧,所得固体物质的化学式为 。
(3) 若D为强电解质溶液,A和C在溶液中反应生成白色沉淀B,则A和C反应的离子方程式为 ;符合此条件的D物质可能是 (填序号)
A.H2SO4 B.CH3COOH C. NaOH D.NH3·H2O E.BaCl2
查看习题详情和答案>>
(15分)A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分产物省略)。请按要求回答下列问题:
(1) 若A是氯碱工业的一种重要产品,通常状况下D是一种非极性气体分子,则D的结构式为 ,A与D以物质的量3:2反应后的溶液中离子浓度的大小顺序为:
(2) 若D为某金属单质,向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为 ;将B的溶液加热蒸干再灼烧,所得固体物质的化学式为 。
(3) 若D为强电解质溶液,A和C在溶液中反应生成白色沉淀B,则A和C反应的离子方程式为 ;符合此条件的D物质可能是 (填序号)
A.H2SO4 B.CH3COOH C. NaOH D.NH3·H2O E.BaCl2
查看习题详情和答案>>
(15分)A、B、C均为中学化学常见的单质,其中一种是金属,通常状况下,A为固体,B为黄绿色气体,C为气体,其余均为化合物,X是一种常用的具有挥发性的无氧强酸,E为黑色固体,H为无色液体,它们之间的转化关系如图(其中某些反应条件和产物已略去)。
(1)写出:A的化学式 ,F的化学式 。
(2)在反应①~⑦中,不属于氧化还原反应的是 (填序号)。
(3)完成:E和X反应的离子方程式: ;
(4)完成H和某种化合物快速制C的化学方程式 
 ,每生成0.15molC电子转移 mol。
,每生成0.15molC电子转移 mol。
(5)B蒸气与过量氨气混合有白烟及另一种气体单质产生,该反应的化学方程式为:
。
(本小题15分) A、B、C、D四种元素原子核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:
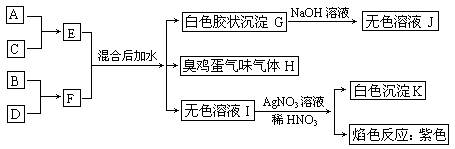
(1)写出四种元素元素符号:A、____B、____C、____D、____。
(2) F的电子式:_________________。
(3)写出E、F混合后加水的化学方程式:_________________________________。
(4)写出GJ的化学方程式:_________________________________。
(5)写出C单质与H水溶液反应的离子方程式:_____________________________。
查看习题详情和答案>>(15分)A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
A B
B C
C D
D
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,则A、D分别为(填写化学式)。
A ,D 。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红,则A为
。写出A B转化的化学方程式:
。
B转化的化学方程式:
。
(3)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则A是 ,
B是 ,C是 。C可作为呼吸面具的填充剂,C与二氧化碳发生反应的化学方程式为: 。A跟水发生反应的化学方程式 。
(4)若A为常见的非金属单质,则A有多种情况,请填写下表,并完成相应的化学反应方程式。(可以不填满,也可以补充)
|
编号 |
A |
· B—C化学方程式 |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
查看习题详情和答案>>