题目内容
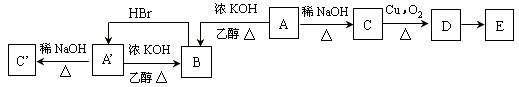
(本小题15分) A、B、C、D四种元素原子核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:
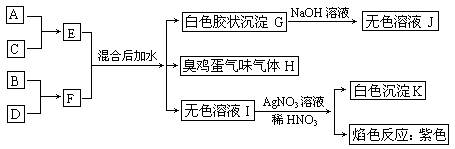
(1)写出四种元素元素符号:A、____B、____C、____D、____。
(2) F的电子式:_________________。
(3)写出E、F混合后加水的化学方程式:_________________________________。
(4)写出GJ的化学方程式:_________________________________。
(5)写出C单质与H水溶液反应的离子方程式:_____________________________。
(1) Al S Cl K(4分)
(2) ![]() (2分)
(2分)
(3) 2AlCl3+3K2S+3H2O=2Al(OH)3↓+3H2S↑+6KCl(3分)
(4) Al(OH)3+NaOH=NaAlO2+2H2O(3分)
(5) Cl2+H2S=S↓+2H++2Cl- (3分)
解析:
考查盐类的双水解,两性氢氧化物,卤离子的检验,焰色反应等知识以及综合应用能力、分析判断与逻辑推理能力,同时考查学生的化学用语等。框图中有几个特征的反应现象:a 臭鸡蛋气味气体;b 白色胶状沉淀溶于NaOH溶液;c 先加AgNO3溶液,再加稀HNO3产生白色沉淀;d 焰色反应:紫色;可分别得出气体是H2S、白色胶状沉淀是Al(OH)3、无色溶液I是KCl。技能空间:常见的特征反应现象及对应物质:
⑴焰色反应:Na黄色,K紫色(透过钴玻璃)。
⑵有臭鸡蛋气味或能使湿润的Pb(Ac)2试纸变黑的气体是H2S。
⑶在空气中由无色迅速变为红棕色的气体是NO。
⑷使品红溶液褪色的往往是SO2 (Cl2使品红溶液褪色后不恢复) 。
⑸能使淀粉变蓝的是I2。
⑹与碱溶液反应生成白色沉淀且放置空气中变灰绿色最终变红褐色的离子是Fe2+。
⑺滴入SCN- 溶液显血红色以及遇苯酚显紫色的离子是Fe3+。
⑻既能跟酸反应又能跟碱反应且生成气体的物质一般是Al,NH4HCO3 ,(NH4)2CO3 ,NH4HSO3,(NH4)2SO3,(NH4)2S,NH4HS。
⑼能使湿润的红色石蕊试纸变蓝的气体是NH3。
⑽与碱反应产生气体的物质是Al、Si、铵盐,产生气体一般是H2、NH3。
⑾与水反应产生气体的物质一般是Na 、F2 、Na2O2。
⑿既能与酸反应又能与碱反应的物质是Al 、Al2O3、Al(OH)3、弱酸弱碱盐、弱酸的酸式盐。
⒀既产生沉淀又产生气体的物质一般是CaC2、Al2S3、Mg3N2 与H2O; S2O32-与H+;CO32-、HCO3-、 SO32-、 HSO3-、 S2-、HS- 与Al3+;CO32-、HCO3-与Fe3+。
应试策略:有些框图推断题,从题干看,基本得不出什么直接的结论。框图中的特征反应及现象往往是解决问题的突破口即题眼。解题时可从上述特征反应及现象直按入手,结合框图中提供的转化关系,往往能迅速得出其他结论。

(本小题15分)为测定空气中CO2含量,做下述实验。
| 配0.1mol/L的标准盐酸和0.01mol/L的标准盐酸 | → | 用0.1mol/L的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60 mL | → | 用Ba(OH)2溶液吸收空气中的CO2 | → | 过 滤 | → | 取滤液20mL,用0.01mol/L的盐酸滴定用去盐酸34.8mL |
(1)为配置标准溶液,请选取必需的一组仪器 。
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A.①②⑤⑥ B.②④⑤⑥⑦ C.②①⑥⑦ D.②④⑤⑥
(2)滴定操作时,左手 ,眼睛注视 。
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤。需过滤的原因是 。
(4)由实验数据算出空气中CO2的体积分数为 。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响) 。