摘要:(1)4NH3 + 5O2 4NO + 6H2O(2)6FeO22― + NO2― + 5H2O = 3Fe2O42― + NH3 + 7OH― 2FeO22― + Cl2 + 8H+ = 2 Fe3+ + 2Cl― + 4H2O
网址:http://m.1010jiajiao.com/timu_id_173128[举报]
 物质结构的多样性让人类使用的材料精彩纷呈.
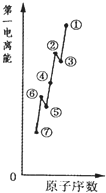
物质结构的多样性让人类使用的材料精彩纷呈.(1)如图是原子序数相连的七种短周期元素第一电离能示意图.其中硼B元素是
(2)乙二酸俗名草酸,是最简单的有机二元酸之一,结构简式为
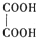 ,草酸钠晶体中存在
,草酸钠晶体中存在A.金属键B.非极性键 C.键D.范德华力 E.氢键 F.离子键
(3)氧化锆(ZrO2)材料具有高硬度,高强度,高韧性,极高的耐磨性及耐化学腐蚀性,氧化锆陶瓷在许多领域获得广泛应用.锆石与钛同族的第五周期元素,锆原子的价电子排布式为
(4)含氧酸可电离的氢原子来自羟基,碳酸的结构式可表达为
(5)PtCl4和氨水反应可获得PtCl4?4NH3,PtCl4?4NH3是一种配合物.100mL0.1mol?L-1 PtCl4?4NH3溶液中滴加足量AgNO3溶液可产生2.87g白色沉淀.该配合物溶于水的电离方程式为
如图是工业生产硝酸的流程.
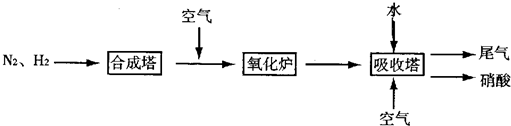
合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

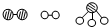 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为 , .
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为 , .
(2)已知N≡N的键能是946kJ?mol-1,H-H的键能为436kJ?mol-1,N-H的键能为393kJ?mol-1,写出合成塔中发生反应的热化学方程式 .
(3)已知4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.8kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ?mol-1;
则热化学方程式N2(g)+O2(g)═2NO(g)△H= kJ?mol-1.
(4)吸收塔中通入空气的目的是 .
查看习题详情和答案>>

合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

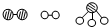 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别为(2)已知N≡N的键能是946kJ?mol-1,H-H的键能为436kJ?mol-1,N-H的键能为393kJ?mol-1,写出合成塔中发生反应的热化学方程式
(3)已知4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.8kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ?mol-1;
则热化学方程式N2(g)+O2(g)═2NO(g)△H=
(4)吸收塔中通入空气的目的是
氨是一种重要的化工产品.其合成原理为N2(g)+3H2(g)?2NH3(g)△H<0.
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1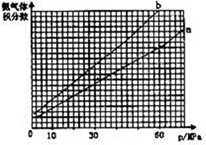
则N2(g)+3H2(g)?2NH3(g)△H= .
(2)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如图.若曲线a对应的温度为500℃,则曲线b对应的温度可能是 .
A.600℃B.550℃C.500℃D.450℃
(3)合成氨所需的氢气可由甲烷与水反应制备.发生反应为:CH4(g)+H2O(g)
CO(g)+3H2(g);△H>0
在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
①表中x= mol?L-1;前2min内CH4的平均反应速率为 .
②反应在3~4min之间,氢气的物质的量增多的原因可能是 (填代号)
A.充入水蒸汽B.升高温度C.使用催化剂D.充入氢气
(4)已知:Kw(H2O)=1.0×10-14、Ksp[A1(OH)3]=1.3×10-33、Kb(NH3?H2O)=1.7×10-5,NH4++[A1(OH)4]-=A1(OH)3↓+NH3?H2O.向含有等物质的量NH4+、A13+、H+的混合溶液中慢慢加NaOH溶液,直至过量,并不断搅拌,依次发生了数个离子反应,其中:第二个离子反应的离子方程式是 ,最后一个离子反应的离子方程式是 .
查看习题详情和答案>>
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ?mol-1;
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1

则N2(g)+3H2(g)?2NH3(g)△H=
(2)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如图.若曲线a对应的温度为500℃,则曲线b对应的温度可能是
A.600℃B.550℃C.500℃D.450℃
(3)合成氨所需的氢气可由甲烷与水反应制备.发生反应为:CH4(g)+H2O(g)
| 催化剂 |
| 加热 |
在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
| t/min | CH4(mol?L-1) | H2O(mol?L-1) | CO(mol?L-1) | H2(mol?L-1) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.3 |
| 3 | n1 | n2 | n3 | 0.3 |
| 4 | 0.09 | 0.19 | x | 0.33 |
②反应在3~4min之间,氢气的物质的量增多的原因可能是
A.充入水蒸汽B.升高温度C.使用催化剂D.充入氢气
(4)已知:Kw(H2O)=1.0×10-14、Ksp[A1(OH)3]=1.3×10-33、Kb(NH3?H2O)=1.7×10-5,NH4++[A1(OH)4]-=A1(OH)3↓+NH3?H2O.向含有等物质的量NH4+、A13+、H+的混合溶液中慢慢加NaOH溶液,直至过量,并不断搅拌,依次发生了数个离子反应,其中:第二个离子反应的离子方程式是
 (2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究.
(2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究.(l)目前合成氨技术原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
如图表示工业合成氨反应在某一段时间中反应速率与反应过程的关系曲线图:
①氢化物的体积分数最高的一段时间为
t0~t1
t0~t1
;t1时刻改变的反应条件是升温
升温
.②NH3极易溶于水,其水溶液俗称氨水.用水稀释0.1mol/L的氨水,溶液中随着水量的增加而减小的是
bd
bd
(填序号).a.
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
(2)1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY冉瓷(能传递H+),实现了高温常压下利用
N2和H2电解合成氨.其阴极的电极反应式
N2+6H++6e-=2NH3
N2+6H++6e-=2NH3
.(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2(g)+6H2O(1)?4NH3(g)+3O2(g)△H=akJ/mol 进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
>
>
0,△S>
>
0,(填“>”“<”或“=”).②已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol;2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol 则2N2(g)+6H2O(g)=4NH3(g)+3O2(g)△H=
+l530kJ/mol
+l530kJ/mol
. 自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.(1)在不同温度下,反应N2(g)+O2(g)?2NO(g)△H=a kJ?mol-1的平衡常数K如下表:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
>
>
0(填“>”、“=”或“<”).②其他条件相同时,在上述三个温度下分别发生该反应.
1538℃时,N2的转化率随时间变化如图所示,请补充完成1760℃时N2的转化率随时间变化的示意图.
(2)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g)?2NO(g)达到平衡时NO的浓度.(此温度下不考虑O2与NO的反应.计算结果保留两位有效数字)
(3)科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.相应的热化学方程式如下:
2N2(g)+6H2O(1)=4NH3(g)+3O2(g)△H=+1530kJ?mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热△H=
(2a-1530)kJ?mol-1
(2a-1530)kJ?mol-1
.(用含a的代数式表示)(4)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定--氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2?2NH3.则在电解法合成氨的过程中,应将H2不断地通入
阳
阳
极(填“正”、“负”、“阴”或“阳”);在另一电极通入N2,该电极反应式为N2+6H++6e-=2NH3
N2+6H++6e-=2NH3
.