网址:http://m.1010jiajiao.com/timu_id_1731036[举报]
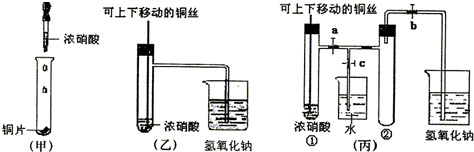
(1)写出铜和浓硝酸反应的离子方程式
(2)和甲装置相比,乙装置的优点有
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操作
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是

(1)甲、乙、丙三个装置中共同发生的化学方程式是________________。?
(2)和甲装置相比,乙装置的优点是①________________,②________________。?
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞________,再打开活塞_______,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应如何操作?________________________。
查看习题详情和答案>>
(1)甲、乙、丙三个装置中共同发生的化学方程式是____________________。
(2)和甲装置相比,乙装置的优点是①___________________,②____________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞__________,再打开活塞__________,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应如何操作?__________________________________。
查看习题详情和答案>>
(1)写出铜和浓硝酸反应的化学方程式:
____________________________________________________________________。
(2)和甲装置相比,乙装置的优点有
____________________________________________________________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹___________,再打开弹簧夹___________,才能使NO2气体充满②试管。
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操作?______________________。
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是___________(气体体积按标准状况计算)。
查看习题详情和答案>>