网址:http://m.1010jiajiao.com/timu_id_1730259[举报]
某温度下,在0.1mol/LnaHB溶液中,已知c(H+)>c(OH―),则下列关系一定正确的( )
A.c(Na+)=0.1mol/L≥c(B2―)
B.c(Na+)=c(HB―)+2c(B2―)+c(OH―)
C.可与0.1mol/LNaOH溶液完全中和
D.c(H+)?c(OH―)=10―14
查看习题详情和答案>>一级电离:H2R2O4
| ||
二级电离:H2R2O4-
| ||
请回答一下问题:
(1)将0.1mol?L-1的NaOH溶液与0.05mol?L-1的H2R2O4溶液等体积混合,冷却至室温测得溶液的pH
(2)NaHR2O4溶液
 H++R2O42-,HR2O4?+H2O
H++R2O42-,HR2O4?+H2O H2R2O4+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性
H2R2O4+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性 H++R2O42-,HR2O4?+H2O
H++R2O42-,HR2O4?+H2O H2R2O4+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性
H2R2O4+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性(3)某温度下,在0.1mol?L-1的NaHR2O4溶液中,以下关系一定不正确的是
A c(H+)?c(OH-)=1×10-14mol2?L-2
B pH>1
C c(OH-)=2c(H2R2O4)+c(HR2
| O | - 4 |
D c(Na+)=0.1mol?L-1≥c(R2
| O | 2- 4 |
 已知H2B在水溶液中存在以下电离:
已知H2B在水溶液中存在以下电离:一级电离:H2B
 H++HB-,二级电离:HB-
H++HB-,二级电离:HB- H++B2-
H++B2-请回答以下问题:
(1)NaHB溶液
 H++B2-,HB?+H2O
H++B2-,HB?+H2O H2B+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性
H2B+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性 H++B2-,HB?+H2O
H++B2-,HB?+H2O H2B+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性
H2B+OH?,因两个平衡程度无法确定,故难以确定溶液酸碱性(2)若0.1mol?L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol?L-1,则H2B的一级电离的电离度为
(3)某温度下,在0.1mol?L-1的NaHB溶液中,以下关系一定不正确的是
A.c(H+)?c(OH-)=1×10-14
B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+)
D.c(Na+)=0.1mol?L-1≥c(B2-)
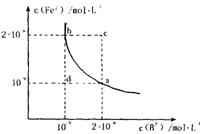
(4)某温度下,FeB(s)
 Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)?c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是
Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)?c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是A.a点对应的KSP等于b点对应的KSP
B.d点无沉淀生成
C.可以通过升温实现由c点变到a点
D.此温度下,KSP=4×10-18.
 已知H2B为二元弱酸,请回答下列问题:
已知H2B为二元弱酸,请回答下列问题:(1)①Na2B溶液呈
②若升高Na2B溶液的温度,则c(HB-)和c(B2-)比值将
(2)某温度下,在0.1mol/L的NaHB溶液中,以下关系一定不正确的是
A.C(H+)?C(OH-)=1×10-14
B.pH>7
C.C(OH-)=2C(H2B)+C(HB-)+C(H+)
D.C(HB-)<0.1mol/L
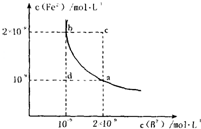
(3)某温度下,FeB在水中的沉淀溶解平衡曲线如图所示.
①写出FeB在水中的沉淀溶解平衡的方程式:
| 溶解 |
| 溶解 |
②该温度下,将FeB固体加入水中,得到的悬浊液中c(Fe2+)为:
③根据图象,下列说法正确的是:
A.a 点对应的Ksp等于b点对应的Ksp
B.通过蒸发可以使溶液由c点变到a点
C.d 点无FeB沉淀生成
D.若改变条件,使FeB的溶解度发生变化,则FeB的Ksp也一定会发生变化.
已知H2B在水溶液中存在以下电离:
![]()
![]() 一级电离:H2B H++HB-,二级电离:HB- H++B2-
一级电离:H2B H++HB-,二级电离:HB- H++B2-
请回答以下问题:
(1)NaHB溶液 (填“呈酸性”、“呈碱性”或“无法确定”),原因是
。
(2)若0.1mol·L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol·L-1,则H2B的一级电离的电离度为 。
(3)某温度下,在0.1mol·L-1的NaHB溶液中,以下关系一定不正确的是 ( )
A.c(H+)·c(OH-)=1×10-14
B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+)
D.c(Na+)=0.1mol·L-1≥c(B2-)
|
的平衡常数表达式为KSP=c(Fe2+)·c(B2-),
FeB在水中的沉淀溶解平衡曲线如右图所示。
下列说法错误的是( )
A.a点对应的KSP等于b点对应的KSP
B.d点无沉淀生成
C.可以通过升温实现由c点变到a点
D.此温度下,KSP=4×10-18
查看习题详情和答案>>