摘要:7.跟100mL0.1mol/(NH4)2 SO4溶液中的NH4+浓度相同的是 ( ) A.01mol/L NH4NO3溶液100ml B.0.2mol/L氨水溶液100ml C.0.2mol/L(NH4)2 CO3溶液50ml D.0.2mol/LNH4CL溶液200ml
网址:http://m.1010jiajiao.com/timu_id_1729690[举报]
下列各组中比值为2:1的是( )
| A、pH均为12的烧碱与Ba(OH)2溶液的物质的量浓度之比 | B、(NH4)2SO4溶液中c(NH4+)与c(SO42-)之比 | C、100mL0.2mol/L的HCl与100mL0.1mol/L的H2SO4溶液中c(H+)之比 | D、相同温度下,0.2mol/L的醋酸溶液与0.1mol/L的醋酸溶液中c(H+)之比 |
草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂.草酸的盐可用作碱土金属离子的广谱沉淀剂.
(1)40℃时混合一定体积的0.1mol/L H2C2O4溶液与一定体积0.01mol/L酸性KMnO4溶液,填写表中空格.
(2)用甲基橙作指示剂,通过酸碱滴定可测定草酸溶液浓度.甲基橙是一种常用的酸碱指示剂,甲基橙(用化学式HIn表示)本身就是一种有机弱酸,其电离方程式为:HIn?H++In-.则酸根离子In-的颜色是 .甲基橙的酸性与草酸相比, (填前者强、前者弱、十分接近、无法判断).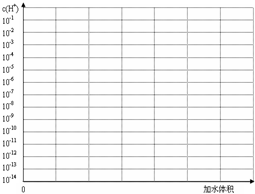
(3)常温下有pH均为3的盐酸和草酸溶液各10ml,加水稀释,在右图画出稀释过程中两种溶液中c(H+)变化的示意图并作必要的标注.
(4)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5mol/L时可认为该离子已沉淀完全.现为了沉淀1L0.01mol/LMgCl2溶液中的Mg2+,加入100mL0.1mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全.
(5)(NH4)2C2O4溶液因NH4+水解程度稍大于C2O42-而略显酸性,0.1mol/L(NH4)2C2O4溶液pH值6.4.现有某未知溶液,常温下由水电离出的c(H+)=1.0×10-5mol/L,该溶液pH可能是 (填字母).
A.5 B.6 C.7 D.9.
查看习题详情和答案>>
(1)40℃时混合一定体积的0.1mol/L H2C2O4溶液与一定体积0.01mol/L酸性KMnO4溶液,填写表中空格.
| 温度 | v(H2C2O4) | v(KMnO4) | KMnO4褪色时间 |
| 40℃ | 10ml | 10ml | 40s |
| 40℃ | 20ml | 20ml |

(3)常温下有pH均为3的盐酸和草酸溶液各10ml,加水稀释,在右图画出稀释过程中两种溶液中c(H+)变化的示意图并作必要的标注.
(4)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5mol/L时可认为该离子已沉淀完全.现为了沉淀1L0.01mol/LMgCl2溶液中的Mg2+,加入100mL0.1mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全.
(5)(NH4)2C2O4溶液因NH4+水解程度稍大于C2O42-而略显酸性,0.1mol/L(NH4)2C2O4溶液pH值6.4.现有某未知溶液,常温下由水电离出的c(H+)=1.0×10-5mol/L,该溶液pH可能是
A.5 B.6 C.7 D.9.
下列溶液中微粒的物质的量浓度关系正确的是( )
| A.Ca(ClO)2溶液中:c(Ca2+)>c(ClO-)>c(OH-)>c(H+) |
| B.等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X-)>c(OH-)=c(H+) |
| C.常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中: c(Cl-)>c(NH4+)> c(NH3·H2O)>c(OH-)>c(H+) |
| D.将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中: |