摘要:9.同体积.同浓度的两份NaOH溶液.分别用pH=2和pH=3的醋酸溶液中和.如恰好完全中和时消耗醋酸溶液的体积依次为V1和V2.则两者的关系正确的是 A.V2>10V1 B.V2<10Vl C.V2=10Vl D.Vl=10V2
网址:http://m.1010jiajiao.com/timu_id_1729671[举报]
向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液
甲和乙;向甲、乙两溶液中分别滴加0.1mol·L-1盐酸,此时反应生成CO2体积(标准状况) 与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )

A.原NaOH溶液的物质的量浓度为0.5 mol·L-1
B.当0<V(HCl)<10mL时,甲溶液中发生反应的离子方程式为: OH-+H+=H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D.乙溶液中滴加盐酸后产生CO2体积的最大值为112mL(标准状况)
查看习题详情和答案>>
某溶液所含溶质是NaOH、Na2CO3、NaHCO3中的一种或两种。取两份等体积的该溶液,分别用酚酞和甲基橙作指示剂,用同浓度的盐酸滴定,当达到滴定终点时消耗盐酸的体积分别为V1和V2,若V1<V2<2V1,则上述溶液中的溶质是( )
A.Na2CO3 B.NaHCO3
C.NaOH和Na2CO3 D.Na2CO3和NaHCO3
查看习题详情和答案>>
向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液
甲和乙;向甲、乙两溶液中分别滴加0.1mol·L-1盐酸,此时反应生成CO2体积(标准状况) 与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )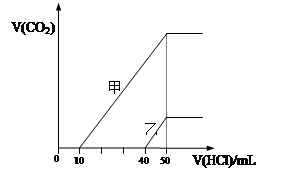
| A.原NaOH溶液的物质的量浓度为0.5 mol·L-1 |
| B.当0<V(HCl)<10mL时,甲溶液中发生反应的离子方程式为: OH-+H+=H2O |
| C.乙溶液中含有的溶质是NaOH、NaHCO3 |
| D.乙溶液中滴加盐酸后产生CO2体积的最大值为112mL(标准状况) |
