摘要:9.某温度下.22g的水中溶解10g胆矾.恰好配成饱和溶液.向该溶液中加入少许无水硫酸铜.充分搅拌后析出晶体2.5g.下列正确的组合是 ( ) A B C D 加入CuSO4的质量(g) 1.6 >1.6 <1.6 <1.6 该温度下CuSO4溶解度(g) 25.00 25.00 25.00 45.45
网址:http://m.1010jiajiao.com/timu_id_1729154[举报]
 已知H2B为二元弱酸,请回答下列问题:
已知H2B为二元弱酸,请回答下列问题:(1)①Na2B溶液呈
碱性
碱性
(填酸性”、碱性”或中性”)②若升高Na2B溶液的温度,则c(HB-)和c(B2-)比值将
增大
增大
(填增大”、减小”或不变”)(2)某温度下,在0.1mol/L的NaHB溶液中,以下关系一定不正确的是
C
C
.A.C(H+)?C(OH-)=1×10-14
B.pH>7
C.C(OH-)=2C(H2B)+C(HB-)+C(H+)
D.C(HB-)<0.1mol/L
(3)某温度下,FeB在水中的沉淀溶解平衡曲线如图所示.
①写出FeB在水中的沉淀溶解平衡的方程式:
FeB(s)
Fe2+(aq)+B2-(aq)
| 溶解 |
FeB(s)
Fe2+(aq)+B2-(aq)
.| 溶解 |
②该温度下,将FeB固体加入水中,得到的悬浊液中c(Fe2+)为:
1.4×10-9
1.4×10-9
mol/L(保留小数点后1位).③根据图象,下列说法正确的是:
AC
AC
.A.a 点对应的Ksp等于b点对应的Ksp
B.通过蒸发可以使溶液由c点变到a点
C.d 点无FeB沉淀生成
D.若改变条件,使FeB的溶解度发生变化,则FeB的Ksp也一定会发生变化.
沉淀溶解平衡也有平衡常数,称为溶度积常数,符号为Ksp,对于某沉淀溶解平衡:
MmAn(s)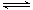 mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
(1)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留在溶液中的c(Fe3+)<10-5 mol·L-1),则溶液的pH最小为 。
(2)某温度时,在100g水中溶解0.74g Ca(OH)2达到饱和,此时溶液的体积约为100 mL,则该温度下Ca(OH)2的溶度积常数Ksp= 。(写出计算过程)
查看习题详情和答案>>
 (2009?深圳二模)某温度下,Ag2SO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
(2009?深圳二模)某温度下,Ag2SO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )