摘要:28.将22.4g铜和氧化铁的混合物粉末加入到浓度为1mol/L的硫酸中.固体恰好完全 溶解.滴入KSCN溶液不显色.此时消耗硫酸体积为VL. (1)硫酸体积V的 L. (2)将所得溶液释释到1L.求此时溶液中金属阳离子物质的最浓度?
网址:http://m.1010jiajiao.com/timu_id_1727933[举报]
将22.4g铜和氧化铁的混合物粉末加入到浓度为1mol/L的硫酸中,固体恰好完全溶解,滴入KSCN溶液不显色,此时消耗硫酸体积为VL。
(1)硫酸体积V的 L。
(2)将所得溶液释释到1L,求此时溶液中金属阳离子物质的量浓度?
查看习题详情和答案>>将22.4g铜和氧化铁的混合物粉末加入到浓度为1 mol•L-1的硫酸中,使之发生反应。
⑴若固体恰好全部溶解,消耗硫酸的体积为V L ,求V的取值范围。
⑵若硫酸溶液过量,反应后溶液的体积为1 L,测得此溶液中Fe2+浓度为0.1 mol•L-1,求原混合物含铜多少克。
查看习题详情和答案>>
将22.4g铜和氧化铁的混合物粉末加入到浓度为1 mol•L-1的硫酸中,使之发生反应。
⑴若固体恰好全部溶解,消耗硫酸的体积为V L ,求V的取值范围。
⑵若硫酸溶液过量,反应后溶液的体积为1 L,测得此溶液中Fe2+浓度为0.1 mol•L-1,求原混合物含铜多少克。
查看习题详情和答案>>

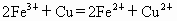 在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.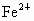 的浓度为0.1mol/L,求原混合物中含铜多少克?
的浓度为0.1mol/L,求原混合物中含铜多少克?
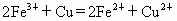 在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.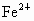 的浓度为0.1mol/L,求原混合物中含铜多少克?
的浓度为0.1mol/L,求原混合物中含铜多少克?