网址:http://m.1010jiajiao.com/timu_id_1727866[举报]
(1)N2(g)+3H2(g) 2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。
2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。

①在1L容器中发生反应,前20min内,v(NH3)= ,放出的热量为 ;
②25min时采取的措施是 ;
③时段III条件下,反应的平衡常数表达式为 (用具体数据表示)。
(2)电厂烟气脱氮的主反应①:4NH3(g)+6NO(g) 5N2(g)+6H2O(g)
△H<0,副反应②:2NH3(g)+8NO(g)
5N2(g)+6H2O(g)
△H<0,副反应②:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g)
△H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是
,导致这种规律的原因是 (任答合理的一条原因)。
5N2O(g)+3H2O(g)
△H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是
,导致这种规律的原因是 (任答合理的一条原因)。

(3)直接供氨式燃料电池是以NaOH溶液为电解质的。电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为 。
查看习题详情和答案>>
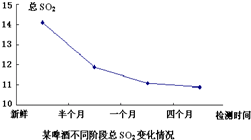 二氧化硫是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系.
二氧化硫是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系.(1)如图是某啤酒样品不同时间阶段总SO2变化情况.
试根据中学所学化学知识分析啤酒样品中总SO2随时间变化的原因之一是
(2)已知甲醛溶液可吸收二氧化硫生成稳定的羟基甲磺酸:HCHO+H2SO3?HO-CH2-SO4H.该有机反应类型属于
(3)啤酒中的二氧化硫可用碘量法进行测定.其原理是:
第一步:先直接用碘标准溶液(0.01mol/L,下同)滴定啤酒样品(10g)中所有还原性物质消耗碘标准溶液V1mL;
第二步:再另取相同质量的啤酒样品加入足量的甲醛溶液,充分反应后再用碘标准溶液滴定,消耗碘标准溶液V2mL;
根据V1和V2可计算出该啤酒中的二氧化硫含量(g/kg)(提示:①SO2+2H2O+I2=2HI+H2SO4;②羟基甲磺酸、甲醛不与I2反应)
请回答:
①碘标准溶液应用
②若进行三次平行实验得到V1和V2的平均值分别是:V1=4.75mL;V2=4.25mL.则该啤酒样品中SO2的含量为
③第二步中加入足量甲醛后约4~6min再进行滴定,若加入甲醛后立即滴定会使测定结果
A.《化学与生活》
(1)现有下列五种物质:(a)食盐 (b)食醋 (c)苹果汁 (d)葡萄糖 (e)青霉素,请按下列要求填空(填序号).
富含维生素C的是
(2)防治环境污染,改善生态环境已成为全球的共识.
①空气质量报告的各项指标可以反映出各地空气的质量.下列气体已纳入我国空气质量报告的是
a.CO2 b.N2 c.NO2
②垃圾应分类收集.导致“白色污染”的生活垃圾应放置于贴有
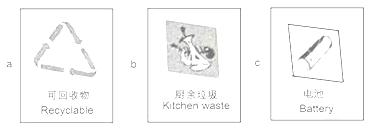
③工业废水需处理达标后才能排放.下列废水处理的方法合理的是
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
(3)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础.请填写下列空格.
①生活中的陶瓷、水泥和
②在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点
③下列对金属制品采取的防护方法不正确的是
A.在电线的外面包上一层塑料层 B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
(4)某肉制品包装上印有相关配料:精选瘦肉、食盐、亚硝酸钠、苯甲酸钠.其中属于调味剂的是
B.《有机化学基础》(我校学生统一不选做)
(1)(3分)根据结构对有机物进行分类,有助于对其性质的掌握.
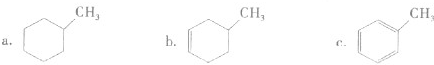
①下列有机物属于芳香烃的是
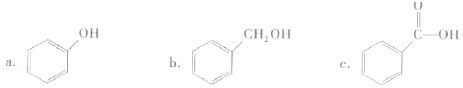
②下列有机物属于酚类的是
③下列有机物属于糖类的是
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为:
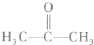
①X的核磁共振氢谱图(H核磁共振谱图)上有
②X的一种同分异构体Y能发生银镜反应,请写出Y的结构简式:
③X的另一种同分异构体z的结构简式为H2C═CHCH2OH,请写出Z与Br2发生加成反应的化学方程式:
(3)2010年上海世博会充分体现了绿色生活理念,节能环保材料在园区内随处可见.如一次性餐盒是由一种生物可降解的高分子合成材料制得.其结构简式如下:
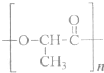
①该高分子材料是由一种单体通过


②若两分子的该单体发生反应,既可能得到环状化合物M,也可能得到链状化合物N.其结构简式如下:
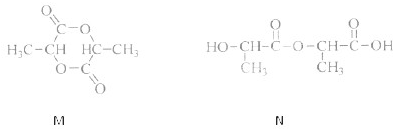
请用两种方法鉴别M和N.方法一:
(2)取10.00g纯碱样品,配成1000mL溶液,取25.00mL放入锥形瓶中,加入某种指示剂,用0.15mol/L的标准盐酸溶液滴定至终点(反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,杂质不与盐酸反应).消耗盐酸体积为30.00mL.试回答下列问题:
取25.00mL溶液所用的仪器是
纯碱样品中碳酸钠的质量分数为
(16分)(Ⅰ)本世纪是生命科学研究的昌盛时期, 科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2-),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中O2-含量,原理是O2-与羟胺反应生成NO2-和一种过氧化物。NO2-在对氨基苯磺酸和α-萘胺作用下,生成粉红的偶氮染体,染体在波长530nm处有显著吸收,且其吸收值与c(NO2-)成正比,从而可计算出样品中的O2-含量。某实验室用以上方法处理后测得溶液中c(NO2-)=2.500×10-3 mol?L-1。
科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2-),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中O2-含量,原理是O2-与羟胺反应生成NO2-和一种过氧化物。NO2-在对氨基苯磺酸和α-萘胺作用下,生成粉红的偶氮染体,染体在波长530nm处有显著吸收,且其吸收值与c(NO2-)成正比,从而可计算出样品中的O2-含量。某实验室用以上方法处理后测得溶液中c(NO2-)=2.500×10-3 mol?L-1。
⑴ 请根据测定原理写出有关反应的离子方程式 ▲ ;
⑵ 计算该样品此时c(O2-) = ▲ ;
⑶ 如用羟胺氧化法测定O2-时,将其生成的过氧化物作为检测物,若选用氧化还原法进行定量分析(用KMnO4标准溶液进行滴定)
① 请写出其测定原理的反应方程式 ▲ ;
② 测定所用的主要玻璃仪器为 ▲ ,通过观察 ▲ 的现象可确定测定反应是否进行完全。
(Ⅱ)水中的NO2-是含氮有机物分解的产物,其浓度的大小是水源污染的标志之一。检测水中的NO2-可用比色法,其步骤是:
a. 配制标准溶液:称取0.30gNaNO2,溶于水后在容量瓶中稀释至1L得溶液A,移取5mL溶液A,稀释至1L,得溶液B。
b. 配制标准色阶:取6只规格为10mL的比色管(即质地、大小、厚薄相同且具塞的平
底试管),分别加入体积不等的溶液B,并稀释至10mL,再加入少许(约0.3g)对苯磺酸粉末,实验结果如下表所示:
| 色阶序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入溶液B的体积(mL) | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
| 反应后溶液颜色 | 由无色变为由浅到深的樱桃红色 | |||||
① 比色法的基本依据是 ▲ ;
② 若水样显色后与色阶中的5号颜色相同,则表明水样中NO2-含量为 ▲ mg/L。
③ 用NaNO2直接配制溶液B的缺点是 ▲ 。
④ 如果水样显色后比6号还深,应采取的措施是 ▲ 。 查看习题详情和答案>>