题目内容
(1)100mL含0.001molCa2+的中性溶液让其通过强酸型阳离子交换膜HR,使Ca2+完全被树脂所交换,再用100mL蒸馏水洗涤树脂到中性,将交换液和洗涤液收集在一起,所得混合液(体积为两者之和)的PH为(2)取10.00g纯碱样品,配成1000mL溶液,取25.00mL放入锥形瓶中,加入某种指示剂,用0.15mol/L的标准盐酸溶液滴定至终点(反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,杂质不与盐酸反应).消耗盐酸体积为30.00mL.试回答下列问题:
取25.00mL溶液所用的仪器是
纯碱样品中碳酸钠的质量分数为
分析:(1)根据电荷守恒计算氢离子的物质的量,再根据c=
计算氢离子浓度,pH=-lgc(H+);
(2)碳酸钠溶液呈碱性,且溶液体积为25.00mL,所以要使用碱式滴定管或移液管量取溶液;
根据盐酸和碳酸钠之间的关系式计算碳酸钠的质量,再根据质量分数公式计算碳酸钠的质量分数.
| n |
| V |
(2)碳酸钠溶液呈碱性,且溶液体积为25.00mL,所以要使用碱式滴定管或移液管量取溶液;
根据盐酸和碳酸钠之间的关系式计算碳酸钠的质量,再根据质量分数公式计算碳酸钠的质量分数.
解答:解:(1)根据电荷守恒得0.001molCa2+应交换出0.002molH+,混合溶液体积=100mL+100mL=200mL,所以c(H+)=
=0.01mol/L,则pH=-lgc(H+)=-lg0.01=2,
故答案为:2;
(2)滴定实验中取样要精确,又因Na2CO3溶液呈碱性,所以宜用碱式滴定管,也可用其他精量仪器如移液管等;
设碳酸钠溶液的物质的量浓度为xmol/L,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
1 2
0.025x 0.03×0.15
x=0.09
n(Na2CO3)=0.09mol/L×1L=0.09mol,
m(Na2CO3)=0.09mol×106g/mol=9.54g
ω(Na2CO3)=
××100%=95.4%,
故答案为:95.4%.
| 0.002mol |
| 0.2L |
故答案为:2;
(2)滴定实验中取样要精确,又因Na2CO3溶液呈碱性,所以宜用碱式滴定管,也可用其他精量仪器如移液管等;
设碳酸钠溶液的物质的量浓度为xmol/L,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
1 2
0.025x 0.03×0.15
x=0.09
n(Na2CO3)=0.09mol/L×1L=0.09mol,
m(Na2CO3)=0.09mol×106g/mol=9.54g
ω(Na2CO3)=
| 9.54g |
| 10g |
故答案为:95.4%.
点评:本题考查了pH的简单计算及滴定实验,明确实验原理是解本题关键,结合物质间的反应、电荷守恒来分析解答,难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
从2L物质的量浓度为1mol?L-1的NaOH溶液中取出100mL溶液,下面关于这100mL溶液的叙述错误的是( )
| A、物质的量浓度为0.1 mol?L-1 | B、物质的量浓度为1 mol?L-1 | C、含4g氢氧化钠 | D、含0.1mol氢氧化钠 |
 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.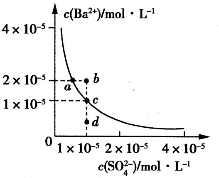 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.请回答下列问题:
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.请回答下列问题: