网址:http://m.1010jiajiao.com/timu_id_1726809[举报]
实验室用碳酸钠粉末配制0.5 mol/L的Na2CO3溶液100 mL,回答下列问题:
(1)所需主要仪器为:天平、药匙、________、________、________、和________.
(2)本实验须称量碳酸钠________g.
(3)下列操作对Na2CO3溶液的物质的量浓度有何影响(填“偏高”、“偏低”、“无影响”).
①摇匀后发现液面低于刻度线再加水:________.
②容量瓶中原有少量蒸馏水:________.
③未用蒸馏水洗涤用过的烧杯和玻璃棒:________.
④定容时俯视观察液面:________.
混合物A由碳酸钠和碳酸氢钠组成.现有两包质量相等的混合物A:
(1)若向其中一包加入100 mL 3 mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200 mL 2 mol/L的稀盐酸,溶液恰好呈中性.
①写出下列反应的离子方程式
碳酸氢钠与过量氢氧化钡的反应:________;
②混合物A中NaHCO3的质量为________g.
(2)若向另一包中先加50 mL 8 mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50 mL 2 mol/L的Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下).混合物A中Na2CO3的质量为________g.
①配制0.100 mol·L-1稀盐酸和0.100 mol·L-1氢氧化钠溶液 ②取一粒药片(药片质量相同,均为0.100 g),研碎后加入20.0 mL蒸馏水 ③以酚酞为指示剂,用0.100 mol·L-1氢氧化钠溶液滴定,用去体积为V时达到终点 ④加入25.00 mL 0.100 mol·L-1稀盐酸
请回答下列问题:
(1)测定过程的正确操作顺序为:______________(填序号)。
(2)测定过程中发生反应的离子方程式为:____________________________________。
(3)若某次实验需重复测定4次。实验室现有50 mL、100 mL、250 mL、500 mL四种规格的容量瓶,则配制稀盐酸应选用的容量瓶规格最好为___________ ,理由是____________________________________。
(4)某同学四次测定的V数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
V/mL | 12.9 | 15.4 | 13.1 | 13.0 |
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数。
目前市场上大量碳酸饮料、矿泉水、食用油等产品包装瓶几乎都是用PET(聚对苯二甲酸乙二醇脂,简称聚酯)制作的.某科学小组利用费聚酯饮料瓶制备对苯二甲酸.部分有机物的性质如下:
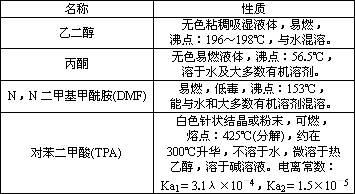
实验过程如下,试回答下列问题:
(1)对苯二甲酸的制备
①在100 mL四颈瓶上分别装置冷凝管、搅拌器和温度计.然后依次加入5.00g废饮料瓶碎片、0.05 g氧化锌、5 g碳酸氢钠和25 mL乙二醇.缓慢搅拌,油浴加热,将温度升至180℃(不超过185℃),在此温度下反应15分钟.
反应过程中的现象是________.
②冷却至160℃左右停止搅拌,将搅拌回流装置改成搅拌、减压蒸馏装置,减压蒸馏.这一步是为了分离出________.
③向四颈瓶中加入50 mL沸水,搅拌使四颈瓶中的残留物溶解.抽滤除去少量不溶物.抽滤需要用到的主要仪器有________.
④将滤液转移到400 mL烧杯中,用25 mL水荡洗滤瓶并倒入烧杯中,再添加水使溶液总体积达200 mL丙酮分2次洗涤,抽干,干燥.
(2)对苯二甲酸含量的测定
称取0.2000 g对苯二甲酸样品于250 mL烧杯中,加入30 mL DMF,搅拌溶解,加入10 mL蒸馏水,搅匀后加4滴酚酞指示剂,用0.1000 mol·L-1氢氧化钠标准溶液滴定,消耗氢氧化钠标准溶液体积为22.60 mL.
滴定终点的现象是________.
所测样品中对苯二甲酸的质量分数为________.
(Ⅰ)下列操作会导致实验结果偏高的是 。
A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线
B.在配制一定物质的量浓度溶液时,用10 mL的量筒量取5.0 mL液体溶质时俯视读数
C.用天平称量20.5 g某物质,砝码和药品的位置放反,所得药品的质量
D.配制一定物质的量浓度的溶液时,定容时俯视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:
a铁架台(含铁圈、铁夹);b锥形瓶;c滴定管;d烧杯(若干);e玻璃棒;f胶头滴管;g托盘天平(含砝码);h滤纸;i量筒;j漏斗;k温度计
现有下列试剂:
A.NaOH固体 B.碳酸钠溶液
C.氯化镁溶液 D.蒸馏水
试填空:
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是 。
A.①是量筒,读数为1.5 mL
B.②是量筒,读数为2.50 mL
C.③是滴定管,读数为2.50 mL
D.①是温度计,读数是1.50 ℃
(2)配制100 mL 0.1 mol·L-1的氢氧化钠溶液时,还缺少的仪器有 。
(3)除去Mg(OH)2中混有的少量Ca(OH)2,可以用到的试剂是 (选填序号),操作方法是 、 、洗涤。
完成上述操作,上述仪器或用品用到的有 (从上述仪器或用品中选择,填上相应序号)。