网址:http://m.1010jiajiao.com/timu_id_1725383[举报]
(10分)有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
(1)E元素原子基态时的外围电子排布式为 。
(2)A2F分子中F原子的杂化类型是 ,F的气态氧化物FO3分子的键角为 。
(3)CA3极易溶于水,其原因是 ,试判断CA3溶于水后,形成CA3·H2O的最合理结构为 (选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为 ;
该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是 (只要求列出算式)。
查看习题详情和答案>>
(10分)有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。

(1)E元素原子基态时的外围电子排布式为 。
(2)A2F分子中F原子的杂化类型是 ,F的气态氧化物FO3分子的键角为 。
(3)CA3极易溶于水,其原因是 ,试判断CA3溶于水后,形成CA3·H2O的最合理结构为 (选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为 ;

该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是 (只要求列出算式)。
查看习题详情和答案>>
 物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
(1)E元素原子基态时的外围电子排布式为 。
(2)A2F分子中F原子的杂化类型是 ,F的气态氧化物FO3分子的键角为 。
(3)CA3极易溶于水,其原因是 ,试判断CA3溶于水后,形成CA3·H2O的最合理结构为 (选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为 ;

该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是 (只要求列出算式)。
(10分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同的短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数1∶1或2∶1形成化合物;B、C分别能与D按原子个数1∶1或1∶2形成化合物
(1)写出只含有A、B、D、E四种元素的两种无结晶水盐的化学式 、 。
(2)如图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 。E与D按原子个数比1∶1形成的化合物的电子式为 。
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F—D | F—F | B—B | F—B | B==D | D==D |
| 键能/ kJ·mol−1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
① 下列三种物质形成的晶体,熔点由高到低的顺序为 (用a、b、c表示)。
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
② 试写出F单质晶体的燃烧的热化学方程式: 。
查看习题详情和答案>>
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素。它们之间的关系如下:
Ⅰ.原子半径:A < C < B < E< D
Ⅱ.原子的最外层电子数:A = D C= E A + B = C
Ⅲ.原子的核外电子层数:B = C = 2A
Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式 ;
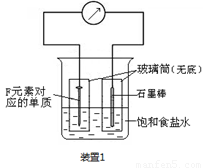
(2)写出某黑色含F的磁性氧化物与E最高价氧化物对应水化物的稀溶液反应的离子方程式: 。装置1经过一段时间向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。单质F发生 (填电化学腐蚀类型)
(3)向A、B、C三种元素组成的某盐稀溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为 ,已知该盐溶液常温下呈酸性,则0.1mol/L该盐溶液中离子浓度的大小顺序为 。
(4)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2。则该复
盐的化学式为 。为检验该复盐中的某种有色离子存在,请写出实验的操作步骤和现象
。
查看习题详情和答案>>