题目内容
(10分)有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。

(1)E元素原子基态时的外围电子排布式为 。
(2)A2F分子中F原子的杂化类型是 ,F的气态氧化物FO3分子的键角为 。
(3)CA3极易溶于水,其原因是 ,试判断CA3溶于水后,形成CA3·H2O的最合理结构为 (选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为 ;

该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是 (只要求列出算式)。
【答案】
(1)3d104s1;(2)sp3;120°;
(3)与水分子间形成氢键、两者都是极性分子、与水反应 (1分,答到一点就可);b;
(4)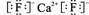 (2分);
(2分); (3分,没带单位不扣分);
(3分,没带单位不扣分);
【解析】略

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目





