摘要:10.向一定量的K2 CO3溶液中缓缓滴加稀盐酸.并不断搅拌.随着盐酸的加入.溶液中离子的数目也相应地发生变化.如图所示.四条曲线与溶液中离子的对应关系完全正确的是 a b c d A Cl- K+ CO32- HCO3- B K+ CO32- Cl- HCO3- C K+ CO32- HCO3- Cl- D K+ HCO3- Cl- CO32-
网址:http://m.1010jiajiao.com/timu_id_1725004[举报]
向一定量的K2CO3溶液中缓缓滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中相关离子的数目也相应地发生变化  (如图)。图中各条曲线与溶液中离子数目的变化对应关系中,正确的是
(如图)。图中各条曲线与溶液中离子数目的变化对应关系中,正确的是
A、NS:K+,MP:H+,QR:CO32-,OT:HCO3-,RU:Cl-
B、NS:K+,MP:CO32-;OQR:HCO3-,OT:Cl-,RU:H+
C、NS:K+,MP:Cl-,QR:H+,OT:HCO3-,RU:CO32-
D、NS:K+,MP:H+,OQR:Cl-,OT:CO32-,RU:HCO3-
查看习题详情和答案>>下列说法正确是( )
A、标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量浓度为
| ||
| B、标准状况下,将64g铜片投入到含2mol H2SO4的浓硫酸中加热会产生22.4L的SO2气体 | ||
| C、向1mol的碳酸钾固体中缓缓滴加含1mol溶质的稀盐酸会产生1mol的CO2气体 | ||
| D、向含有1mol Ba(OH)2溶液中通入足量CO2气体产生1mol BaCO3白色沉淀 |
 无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另外一种固体.某学生将无水亚硫酸钠受热后的试样溶于水制成浓溶液,用下图所示的实验装置进行实验,他向试样溶液中缓缓地逐滴加入稀盐酸,根据实验现象判断固体试样含有什么成分?(已知:Na2 S+2HCl═2NaCl+H2S+SO2+2H2S═3S+2H2 O)
无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另外一种固体.某学生将无水亚硫酸钠受热后的试样溶于水制成浓溶液,用下图所示的实验装置进行实验,他向试样溶液中缓缓地逐滴加入稀盐酸,根据实验现象判断固体试样含有什么成分?(已知:Na2 S+2HCl═2NaCl+H2S+SO2+2H2S═3S+2H2 O)(1)无水亚硫酸钠受热分解的化学方程式是
4Na2SO3=Na2S+3Na2SO4
4Na2SO3=Na2S+3Na2SO4
,装置中的NaOH溶液的作用是吸收H2S或SO2气体
吸收H2S或SO2气体
.(2)如果加热温度在600℃以上,再向所得固体的试样溶液中缓缓滴加稀盐酸至足量,观察到CuSO4溶液中出现黑色沉淀,试分析其他装置中可能出现的现象.试样溶液:
有淡黄色沉淀生成,并有气泡冒出
有淡黄色沉淀生成,并有气泡冒出
,解释这种现象的离子方程式是SO32-+2S2-+6H+=3S↓+3H2O,S2-+2H+=H2S↑
SO32-+2S2-+6H+=3S↓+3H2O,S2-+2H+=H2S↑
;品红溶液:有气泡生成但不褪色
有气泡生成但不褪色
,出现这种现象的原因是:加热后固体中所含的Na2SO3和Na2S的物质的量之比小于1:2,在酸性溶液中反应产生的气体只含H2S,而不含SO2
加热后固体中所含的Na2SO3和Na2S的物质的量之比小于1:2,在酸性溶液中反应产生的气体只含H2S,而不含SO2
.(3)若加入了足量的稀盐酸后,品红溶液和CuSO4溶液中仍无明显的现象发生,原因是
加热后固体中所含Na2SO3和Na2S的物质的量之比等于1:2,在酸性溶液中恰好生成S,不产生H2S和SO2
加热后固体中所含Na2SO3和Na2S的物质的量之比等于1:2,在酸性溶液中恰好生成S,不产生H2S和SO2
.
为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和如下图所示的实验装置进行实验.请回答下列有关问题:
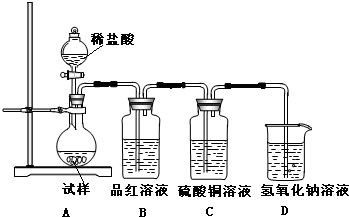
(1)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体.如果加热温度低于600℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中HSO3-的物质的量浓度变化趋势为 ;
(2)如果加热温度为700℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则反应生成淡黄色沉淀的离子方程式为 ;此时在B、C两装置中可能观察到的现象为 或 .
(3)在(2)中滴加足量盐酸后,烧瓶内除Cl-外,还存在另一种浓度较大的阴离子(X)为 .检验该阴离子(X),先取固体试样溶于水配成溶液,为了加速固体试样的溶解,可采取 措施.以下是检验阴离子(X)的两种实验方案,你认为合理的方案是 (填“甲”或“乙”).
方案甲:取少量试样溶液于试管中,先加稀HNO3,再加BaCl2溶液,有白色沉淀生成,证明该离子存在.
方案乙:取少量试样溶液于试管中,先加稀HCl,再加BaCl2溶液,有白色沉淀生成,证明该离子存在.
(4)写出Na2SO3固体加热到600℃以上分解的化学方程式 .
查看习题详情和答案>>

(1)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体.如果加热温度低于600℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中HSO3-的物质的量浓度变化趋势为
(2)如果加热温度为700℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则反应生成淡黄色沉淀的离子方程式为
(3)在(2)中滴加足量盐酸后,烧瓶内除Cl-外,还存在另一种浓度较大的阴离子(X)为
方案甲:取少量试样溶液于试管中,先加稀HNO3,再加BaCl2溶液,有白色沉淀生成,证明该离子存在.
方案乙:取少量试样溶液于试管中,先加稀HCl,再加BaCl2溶液,有白色沉淀生成,证明该离子存在.
(4)写出Na2SO3固体加热到600℃以上分解的化学方程式