网址:http://m.1010jiajiao.com/timu_id_172490[举报]
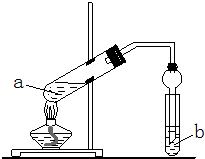
 某同学为验证Fe能与热的浓HNO3反应,设计了如上图所示的实验装置,a中加入的是Fe片和浓HNO3,b加入的是NaOH溶液.请你参与研究并回答下列问题:
某同学为验证Fe能与热的浓HNO3反应,设计了如上图所示的实验装置,a中加入的是Fe片和浓HNO3,b加入的是NaOH溶液.请你参与研究并回答下列问题:(1)当该同学实验结束时,铁完全溶解,试管液面上方为无色气体,试管上部为红棕色气体,此时用所得的溶液又进行如下试验和探究:
①在所得的溶液中加入一小块Cu片,结果Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解.Cu片溶解的原因可能是
②请设计实验证明再加入Cu片不再溶解后的溶液中含有Fe2+但不含Fe3+.说明具体操作和实验现象
(2)若研究稀硝酸与铁的反应,要用浓硝酸进行配制.实验室有10mol/L 的硝酸溶液,从中量出5.0mL,其物质的量浓度为
(1)当该同学实验结束时,铁完全溶解,试管液面上方为无色气体,试管上部为红棕色气体,此时用所得的溶液又进行如下试验和探究:
①在所得的溶液中加入一小块Cu片,结果Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解.Cu片溶解的原因可能是______、
______(用离子方程式表示).
②请设计实验证明再加入Cu片不再溶解后的溶液中含有Fe2+但不含Fe3+.说明具体操作和实验现象______.
(2)若研究稀硝酸与铁的反应,要用浓硝酸进行配制.实验室有10mol/L的硝酸溶液,从中量出5.0mL,其物质的量浓度为______mol/L.现将量出的5.0mL硝酸溶液配制成0.50mol/L的稀硝酸,所需要的玻璃仪器除烧杯、玻璃棒外,还需要______和______.在配制过程中,定容时仰视,则所配溶液的浓度______(填“偏大”或“偏小”或“无影响”).
如下图,一定温度下,分别往容积均为5L的甲(恒压容器)、乙(恒容容器)中加入0.5mol无色的![]() 气体,立即出现红棕色。当反应进行到2s时,测得乙容器中
气体,立即出现红棕色。当反应进行到2s时,测得乙容器中![]() 的浓度为0.09mol·
的浓度为0.09mol·![]() 。经过60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)
。经过60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)

(1)容器中气体出现红棕色的原因(用化学方程式表示)是:_________________________
_______________________________________________________.
(2)前2s内乙容器中以![]() 的浓度变化表示的反应速率为________.
的浓度变化表示的反应速率为________.
(3)达到平衡时,甲容器中反应所需的时间________60s(填“大于”、“小于”或“等于”,以下同);容器内![]() 的浓度甲________乙;反应过程中吸收的能量甲________乙.
的浓度甲________乙;反应过程中吸收的能量甲________乙.
(4)若要使甲、乙中![]() 浓度相等,不能采取的措施是________(填选项的标号).
浓度相等,不能采取的措施是________(填选项的标号).
A.保持温度不变,适当压缩甲容器体积
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量![]()
查看习题详情和答案>>

(1)容器中气体出现红棕色的原因(用化学方程式表示)是:_________________________
_______________________________________________________.
(2)前2s内乙容器中以![]() 的浓度变化表示的反应速率为________.
的浓度变化表示的反应速率为________.
(3)达到平衡时,甲容器中反应所需的时间________60s(填“大于”、“小于”或“等于”,以下同);容器内![]() 的浓度甲________乙;反应过程中吸收的能量甲________乙.
的浓度甲________乙;反应过程中吸收的能量甲________乙.
(4)若要使甲、乙中![]() 浓度相等,不能采取的措施是________(填选项的标号).
浓度相等,不能采取的措施是________(填选项的标号).
A.保持温度不变,适当压缩甲容器体积
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量![]()
查看习题详情和答案>>
 如图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色.当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol?L-1.经过 60s,乙容器中的反应达到平衡.(反应过程中两个容器的温度均保持恒定)
如图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色.当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol?L-1.经过 60s,乙容器中的反应达到平衡.(反应过程中两个容器的温度均保持恒定)(1)容器中气体出现红棕色的原因(用化学方程式表示)是:
(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为
(3)达到平衡时,甲容器中反应所需的时间