网址:http://m.1010jiajiao.com/timu_id_1721431[举报]
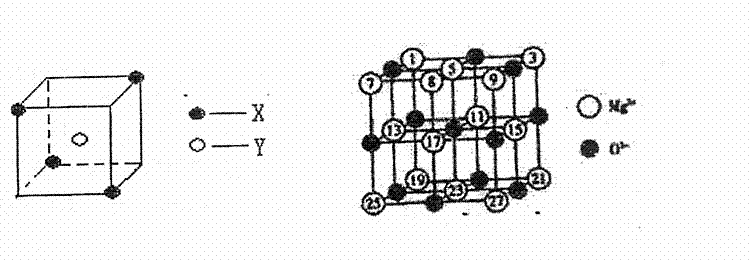
某离子晶体晶胞结构如右图所示,X位于立方体的顶点,Y位于立方体的中心,试回答:
(1)晶体中每个Y同时吸引着 个X,每个X同时吸引着 个Y,该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有 个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为(填角的度数) 。
(4)设该晶体的摩尔质量为M g?mol-1,晶体密度为ρg?cm-3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。
查看习题详情和答案>>(1)某离子晶体晶胞结构单元如图所示,X位于立方体的顶点,Y位于立方体的中心
①晶体中每个Y同时吸引着 个X,每个X同时吸引着 个Y,该晶体的化学式是 。
②晶体中每个X周围与它最接近且距离相等的X共有 个。
③某气态分子也具有上图所示的空间结构,该分子的化学式是 。
![]() (2)已知MEO的晶体结构属于NaC1型。某同学画出的MgO晶胞结构示意图如右图所示,请改正图中错误: .
(2)已知MEO的晶体结构属于NaC1型。某同学画出的MgO晶胞结构示意图如右图所示,请改正图中错误: .
![]()
![]()
 查看习题详情和答案>>
查看习题详情和答案>>
晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体结构如右图所示。 随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取m gNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
⑴步骤①中A仪器最好用__________________(填序号)。
A.量筒 B.烧杯 C.容量瓶 D.试管
(2)步骤②中是用酸式滴定管还是用碱式滴定管 ,
⑶能否用水代替苯______ ???_,其原因是_________ __________
⑷经X射线衍射测得NaCl晶胞中最邻近的Na+ 和Cl- 平均距离为a cm,则利用上述
方法测得的阿伏加德罗常数的表达式为NA=_______________________ 。
⑸纳米材料的表面原子占原子数的比例极大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分比为_________________(保留一位小数)。
⑴C (2)酸式滴定管;(3)否; 水会溶解NaCl,不能准确测出NaCl固体的体积
(4)NA=
(5) 96.3%
查看习题详情和答案>>(15分)【物质结构与性质】
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2 np2,B元素原子的最外层鬼子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中有 个δ键、 个π键. A6H6分子中A原子的杂化轨道类型是 杂化.
(2)当n=3时,A与B形成的晶体属于 晶体.
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是 (用元素符号表示);A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示).
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O.该配合物中的中心离子钴离子
在基态时的核外电子排布式为 .作为配位体之一的NH3分子的空间构型为
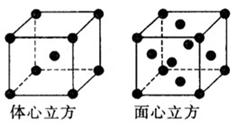
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
查看习题详情和答案>>
(15分)【物质结构与性质】
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2 np2,B元素原子的最外层鬼子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中有 个δ键、 个π键. A6H6分子中A原子的杂化轨道类型是 杂化.
(2)当n=3时,A与B形成的晶体属于 晶体.
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是 (用元素符号表示);A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示).
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O.该配合物中的中心离子钴离子
在基态时的核外电子排布式为 .作为配位体之一的NH3分子的空间构型为
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为