摘要:配制0.1mol·L-1的NaOH溶液时.下列操作会导致实际浓度偏高的是 . A.使用的砝码部分生锈 B.定容时俯视容量瓶的刻度线 C.选用的容量瓶内残留有少量蒸馏水 D.定容.摇匀后.发现液面低于刻度线.再加水至刻度线 (2)按要求填空: ①用已准确称量的10.6gNa2CO3固体配制1.00mol·L-1 Na2CO3溶液100mL.所需要的仪器为 . ②除去Na2CO3固体中混有少量的KNO3.选择的除杂方法为 法.
网址:http://m.1010jiajiao.com/timu_id_1719808[举报]
用实验确定某酸HB的弱电解质.两同学的方案是:
甲:
①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质.
乙:
①用已知物质的量浓度的HB溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH
A.HCl溶液的试管中放出H2的速率快;
B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快.
(3)请你评价:乙方案中两个难以实现之处
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达.
查看习题详情和答案>>
甲:
①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质.
乙:
①用已知物质的量浓度的HB溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是
100mL的容量瓶
100mL的容量瓶
.(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH
>
>
1(选填>、<、=)乙方案中,说明HB是弱电解质的现象是B
B
(多选扣分).A.HCl溶液的试管中放出H2的速率快;
B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快.
(3)请你评价:乙方案中两个难以实现之处
配制pH=1的HA溶液难以实现,加入锌粒难以做到表面积相同
配制pH=1的HA溶液难以实现,加入锌粒难以做到表面积相同
.(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达.
配制NaB溶液,测定溶液的pH>7,证明HB为弱电解质
配制NaB溶液,测定溶液的pH>7,证明HB为弱电解质
.(2009?南京二模)某种胃药中止酸剂为CaCO3.为测定其中CaCO3含量,某研究小组设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答有关问题:
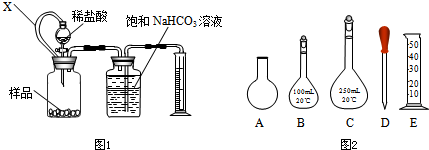
(1)方案一:用如图1装置测量一定量样品与足量稀盐酸反应生成CO2的体积,计算CaCO3的含量;装置中连通管X的作用是
(2)方案二:用滴定法测定,有以下几步操作:
A.配制0.100mol/L HCl溶液和0.100mol/L NaOH溶液
B.取一粒药片(0.100g),研碎后加入20.0mL蒸馏水
C.以酚酞为指示剂,用0.100mol/L NaOH溶液滴定,用去体积为VmL达到终点
D.用酸式滴定管加入25.00mL 0.100mol/L HCl溶液,充分反应
①测定过程的正确操作顺序为
②现需要重复滴定4次,配制0.1mol/L HCl溶液需要选用图2所示仪器中的
③经测定,每次消耗NaOH溶液体积的平均值为13.00mL,则该胃药中CaCO3的质量分数
④与方案一相比,方案二的主要优点是
查看习题详情和答案>>

(1)方案一:用如图1装置测量一定量样品与足量稀盐酸反应生成CO2的体积,计算CaCO3的含量;装置中连通管X的作用是
使广口瓶与分液漏斗内气体压强相同,便于滴入酸液
使广口瓶与分液漏斗内气体压强相同,便于滴入酸液
、消除滴入盐酸体积对所测气体体积的影响
消除滴入盐酸体积对所测气体体积的影响
.(2)方案二:用滴定法测定,有以下几步操作:
A.配制0.100mol/L HCl溶液和0.100mol/L NaOH溶液
B.取一粒药片(0.100g),研碎后加入20.0mL蒸馏水
C.以酚酞为指示剂,用0.100mol/L NaOH溶液滴定,用去体积为VmL达到终点
D.用酸式滴定管加入25.00mL 0.100mol/L HCl溶液,充分反应
①测定过程的正确操作顺序为
ABDC 或BADC
ABDC 或BADC
(填字母).②现需要重复滴定4次,配制0.1mol/L HCl溶液需要选用图2所示仪器中的
CD或CDE
CD或CDE
(填字母).③经测定,每次消耗NaOH溶液体积的平均值为13.00mL,则该胃药中CaCO3的质量分数
60%
60%
.④与方案一相比,方案二的主要优点是
滴定法所需样品和试剂量少,实验测定结果误差小
滴定法所需样品和试剂量少,实验测定结果误差小
.实验室欲配制0.1mol/L的NaOH溶液500mL.回答下列问题:
(1)配制时,必须使用的容量瓶的规格是
(2)配制溶液时,需NaOH的质量
(3)在配制0.1mol/L的NaOH溶液500mL的实验中,以下操作中会引起所配NaOH溶液浓度偏高的是
A.定容时俯视刻度线
B.转移溶液时,不慎将溶液洒到容量瓶外
C.容量瓶中原有少量蒸馏水
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线
(4)将500mL0.1mol/LNaOH溶液稀释到1000mL,则稀释后溶液中NaOH的物质的量浓度是
查看习题详情和答案>>
(1)配制时,必须使用的容量瓶的规格是
500
500
mL,该实验中两次用到玻璃棒,其作用分别是搅拌
搅拌
,引流
引流
.(2)配制溶液时,需NaOH的质量
2.0
2.0
g.(3)在配制0.1mol/L的NaOH溶液500mL的实验中,以下操作中会引起所配NaOH溶液浓度偏高的是
A
A
.A.定容时俯视刻度线
B.转移溶液时,不慎将溶液洒到容量瓶外
C.容量瓶中原有少量蒸馏水
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线
(4)将500mL0.1mol/LNaOH溶液稀释到1000mL,则稀释后溶液中NaOH的物质的量浓度是
0.05
0.05
mol/L.
用实验确定某酸HA是弱电解质.两同学的方案是:
甲:①称取一定质量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是 .
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快.
(3)甲方案的第②步中用pH试纸测定溶液pH的操作是 .
(4)丙同学认为乙方案中存在难以实现之处和不妥之处.难以实现之处是 ;不妥之处是 .
(5)若该酸为醋酸,常温下用6.0g醋酸配制的溶液与 NaOH溶液完全中和时放出的热量是a kJ/mol,该反应的热化学方程式是 .
查看习题详情和答案>>
甲:①称取一定质量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH
乙方案中,说明HA是弱电解质的现象是
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快.
(3)甲方案的第②步中用pH试纸测定溶液pH的操作是
(4)丙同学认为乙方案中存在难以实现之处和不妥之处.难以实现之处是
(5)若该酸为醋酸,常温下用6.0g醋酸配制的溶液与 NaOH溶液完全中和时放出的热量是a kJ/mol,该反应的热化学方程式是
甲、乙两同学拟用实验确定某酸HA是弱电解质.他们的方案分别是:
甲:①称取一定质量的HA配制0.1mol/L的溶液100mL;②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH
(3)乙方案中,说明HA是弱电解质的现象是
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),并作简明扼要表述:
查看习题详情和答案>>
甲:①称取一定质量的HA配制0.1mol/L的溶液100mL;②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是
100mL容量瓶
100mL容量瓶
.(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH
>
>
1(选填“>”、“<”或“=”).简要说明pH试纸的使用方法:取一小段pH试纸放在玻璃片上,用玻璃棒蘸取待测液点在pH试纸中央,对照比色卡,读出溶液的pH
取一小段pH试纸放在玻璃片上,用玻璃棒蘸取待测液点在pH试纸中央,对照比色卡,读出溶液的pH
.(3)乙方案中,说明HA是弱电解质的现象是
装HA溶液的试管中放出H2的速率快
装HA溶液的试管中放出H2的速率快
.(4)请你再提出一个合理而比较容易进行的方案(药品可任取),并作简明扼要表述:
用蒸馏水配制少量NaA溶液,再测其pH,若pH>7,说明HA是弱电解质
用蒸馏水配制少量NaA溶液,再测其pH,若pH>7,说明HA是弱电解质
.