摘要:在1升浓度为c摩/升的弱酸HA溶液中,HA.H+和A-的物质的量之和为nc摩,则HA的电离度是 [ ]
网址:http://m.1010jiajiao.com/timu_id_1717960[举报]
黄铁矿在高温时和氧气反应生成氧化铁和二氧化硫(假设矿石中的杂质不参与化学反应).某化学学习小组对黄铁矿样品进行如下实验探究:
【实验一】测定硫元素的含量
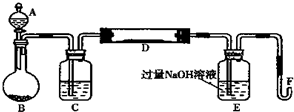
Ⅰ.实验装置如图所示(夹持和加热装置省略).A中的试剂是双氧水,将m1g该黄铁矿样品放入硬质玻璃管D中.从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管中的黄铁矿样品至反应完全.
Ⅱ.反应结束后,将E瓶中的溶液进行如下处理: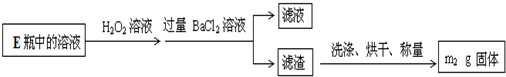
【实验二】测定铁元素的含量
Ⅲ.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250ml;
④每次取稀释液25.00ml,用已知物质的量浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V ml.
请回答下列问题:
(1)仪器B中发生反应的化学方程式是 ;仪器C中装入的试剂是 .E瓶的作用是 .
(2)Ⅱ中加入H2O2发生反应的离子方程式 .
(3)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还必须要有 ;④中取稀释液25.00ml需用的仪器是 .
(4)假设在整个实验过程中硫元素和铁元素没有损失,则该黄铁矿样品中硫元素的质量分数为 .(用含m1和m2的代数式表示);该黄铁矿中铁元素的质量分数为 .(用含m1、c、V的代数式表示)
查看习题详情和答案>>
【实验一】测定硫元素的含量

Ⅰ.实验装置如图所示(夹持和加热装置省略).A中的试剂是双氧水,将m1g该黄铁矿样品放入硬质玻璃管D中.从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管中的黄铁矿样品至反应完全.
Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:

【实验二】测定铁元素的含量
Ⅲ.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250ml;
④每次取稀释液25.00ml,用已知物质的量浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V ml.
请回答下列问题:
(1)仪器B中发生反应的化学方程式是
(2)Ⅱ中加入H2O2发生反应的离子方程式
(3)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还必须要有
(4)假设在整个实验过程中硫元素和铁元素没有损失,则该黄铁矿样品中硫元素的质量分数为
(2013?泸州一模)在高温时硫铁矿(主要成分FeS2)和氧气反应生成三氧化二铁和二氧化硫(假设硫铁矿中的杂质不参与化学反应).某化学研究学习小组对硫铁矿样品进行如下实验探究:
【实验一】测定硫元素的含量
Ⅰ.实验装置如图所示(夹持和加热装置已省略).A中的试剂是双氧水,将mg该硫铁矿样品放入硬质玻璃管D中.从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管D中的硫铁矿样品至反应完全.

Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:

【实验二】测定铁元素的含量
Ⅲ.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解已冷却的硬质玻璃管D中的固体,过滤,得到滤液A;
②在滤液A中加入过量的还原剂使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
③将滤液B稀释为250mL;
④取稀释液25.00mL,用浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL.
请根据以上实验,回答下列问题:
(1)Ⅰ中装置C中盛装的试剂是
(2)Ⅱ中加入过量H2O2溶液发生反应的离子方程式为
(3)Ⅲ的步骤③中,将滤液B稀释为250mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是
(4)假设在整个实验过程中硫元素和铁元素都没有损失,则该硫铁矿样品中硫元素的质量分数为
×100%
×100%.(用含m1和m2的代数式表示)铁元素的质量分数为
×100%
×100%.(用含m1、c、v的代数式表示)
查看习题详情和答案>>
【实验一】测定硫元素的含量
Ⅰ.实验装置如图所示(夹持和加热装置已省略).A中的试剂是双氧水,将mg该硫铁矿样品放入硬质玻璃管D中.从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管D中的硫铁矿样品至反应完全.

Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:

【实验二】测定铁元素的含量
Ⅲ.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解已冷却的硬质玻璃管D中的固体,过滤,得到滤液A;
②在滤液A中加入过量的还原剂使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
③将滤液B稀释为250mL;
④取稀释液25.00mL,用浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL.
请根据以上实验,回答下列问题:
(1)Ⅰ中装置C中盛装的试剂是
浓硫酸
浓硫酸
;E瓶的作用是吸收二氧化硫
吸收二氧化硫
.(2)Ⅱ中加入过量H2O2溶液发生反应的离子方程式为
H2O2+SO32-═SO42-+H2O
H2O2+SO32-═SO42-+H2O
.(3)Ⅲ的步骤③中,将滤液B稀释为250mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是
250mL
250mL
;④中盛装KMnO4溶液的仪器是酸式滴定管
酸式滴定管
.(4)假设在整个实验过程中硫元素和铁元素都没有损失,则该硫铁矿样品中硫元素的质量分数为
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
| 2.8cV |
| m1 |
| 2.8cV |
| m1 |
 某氢氧化钾样品中含有少量不与酸作用的杂质,为了测定其质量分数,进行以下滴定操作:
某氢氧化钾样品中含有少量不与酸作用的杂质,为了测定其质量分数,进行以下滴定操作:A.在250ml的容量瓶中配制250ml的氢氧化钾溶液;
B.将氢氧化钾溶液装入碱式滴定管,调节液面,向锥形瓶中滴入25.00ml氢氧化钾溶液并滴入几滴甲基橙指示剂;
C.在天平上准确称取KOH样品Wg,在烧杯中用蒸馏水溶解;
D.将物质的量浓度为C mol/L的标准硫酸溶液装入酸式滴定管,调节液面记下开始读数为V1;
E.在锥形瓶下垫一张白纸,滴定至橙色为止,记下读数V2.就此完成下列填空:
(1)操作步骤的正确顺序是(用编号字母填)
(2)E步骤的操作中在锥形瓶下垫一张白纸的作用是
便于准确判断终点时颜色的变化情况
便于准确判断终点时颜色的变化情况
;(3)上述B步骤操作之前,若锥形瓶用KOH样品洗涤,则测定的浓度
偏高
偏高
(填“偏高”“偏底”或“不影响”),原因是锥形瓶用KOH样品洗涤,锥形瓶内KOH的物质的量偏大,消耗硫酸的体积偏大
锥形瓶用KOH样品洗涤,锥形瓶内KOH的物质的量偏大,消耗硫酸的体积偏大
.(4)D步骤的操作中液面应调节到
调节到零刻度或零稍下的某一刻度
调节到零刻度或零稍下的某一刻度
;(5)若滴定结束时,滴定管液面如图所示,则终点读数为
21.10
21.10
mL.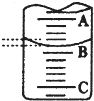 某化学实验小组探究市售食用白醋中醋酸的准确浓度,取25.00 mL某品牌食用白醋于锥形瓶中,在实验室用浓度为cb mol/L的标准NaOH溶液对其进行滴定.
某化学实验小组探究市售食用白醋中醋酸的准确浓度,取25.00 mL某品牌食用白醋于锥形瓶中,在实验室用浓度为cb mol/L的标准NaOH溶液对其进行滴定.(1)如图表示50 mL滴定管中液面的位置,若A与C刻度间相差1 mL,A处的刻度为25,滴定管中液面读数应为
25.40
25.40
mL.(2)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为V mL,NaOH标准液浓度为c mol/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
AB
AB
.A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
C.第一次滴定用的锥形瓶未润洗
D.滴定结束时,俯视读数
(3)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c=
| (23.35+25.30)c |
| 2V |
| (23.35+25.30)c |
| 2V |