网址:http://m.1010jiajiao.com/timu_id_169121[举报]
一、单项选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.D 2.C 3.B 4.D 5.C 6.A 7.B 8.D
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
9.CD 10.AD 11.D 12.C 13.BC 14.D
三、(本题包括1小题,共14分)
15.
方案一:
(1)在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较
(2)排除因盐酸的加入,稀释氢氧化钠溶液而引起pH减小
方案二:
(1)赶走溶液中少量氧气,隔绝氧气
 (2)CO32―+H2O HCO3―+OH―
(2)CO32―+H2O HCO3―+OH―
(3)做对比实验,取上述NaOH溶液稀释,加入酚酞溶液出现红色且不褪去
方案三:
(1)7 (2)U形管中左边液面下降
(每空2分,共14分)
四、(本题包括2小题,共18分)
16.
⑴ 

⑵CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-
⑶Al4SiC4+2N2 4AlN+SiC+
4AlN+SiC+
⑷可行,该反应是一个焓减、熵略大于0的反应,能自发进行
(每空2分,共8分)
17.
⑴ CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
生成的CaCO3溶解度小于CaSO4有利于反应向正向进行。
⑵)BCD ⑶CO2 ⑷ABD(每空2分,共10分)
 五、(本题包括1小题,共10分)
五、(本题包括1小题,共10分)
18.
⑴见图示(2分 ,其中过渡元素涂对得1分)
⑵  ⑶ r(Cl-)>r(K+)
⑶ r(Cl-)>r(K+)
⑷ ②④ (5) 
(除⑴外其余每空2分,共10分)
 六、(本题包括1小题,共10分)
六、(本题包括1小题,共10分)
19.
⑴①增大压强 t3~t4 ②
⑵①如图 ②适当增大压强,研究新催化剂
(每空2分,共10分)
七、(本题包括1小题,共8分)
20.
⑴ 2 第2周期第VIA族 (各1分,共2分)
⑵1s22s22p63s23p63d64s2
⑶H+ + AlO2-
+ H2O Al(OH)3
Al(OH)3 Al3+ + 3H2O
Al3+ + 3H2O
⑷4Fe(OH)2 + 2H2O+ O2=4Fe(OH)3
(除⑴外其余每空2分,共8分)
八、(本题包括1小题,共12分)
21.
⑴-80kJ?mol―1
⑵用过量的稀硫酸溶解过量的镁,不断搅拌,过滤,洗净、干燥
⑶加快反应速率,促进平衡向水解的方向移动
⑷取少量洗涤液,在其中加入AgNO3(或BaCl2),无沉淀生成则说明无相应离子。
Ag++Cl-=AgCl↓ Ba2++SO42-=BaSO4↓
(每空2分,共8分)
Ⅲ 1.5mol/L(4分,分步给分)
 2NH3(g);ΔH=-92 kJ/mol,在一容积为2 L的密闭容器中加入一定量的N2和H2,在一定条件下发生合成氨反应,反应中NH3的物质的量浓度的变化情况如下图
2NH3(g);ΔH=-92 kJ/mol,在一容积为2 L的密闭容器中加入一定量的N2和H2,在一定条件下发生合成氨反应,反应中NH3的物质的量浓度的变化情况如下图
(2)反应达到平衡时,测得NH3占平衡混合气体体积的1/3,则平衡混合气体折合成标准状况下的体积是______ L,反应过程中放出的热量为________ kJ.
(3)平衡时测得N2的物质的量为0.10 mol,则N2的转化率α(N2)=________.
(4)实验测得一定条件下合成氨反应的速率与体系内各物质的浓度有以下关系:v=kc(N2)·c1.5(H2)·c-1(NH3)(k为常数),请根据此速率方程式,结合自己的已有知识对如何提高合成氨反应的速率提出三点建议:_____________________________________.
(1)合成氨反应的热化学方程式:N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,至少在反应混合物中要投放N2的物质的量为________ mol。
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式:__________________________,
负极的电极反应式:__________________________。
(3)如图是一个电解过程示意图。
①锌片上发生的电极反应式是:_______________________
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,至少在反应混合物中要投放N2的物质的量为________ mol。
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式:__________________________,
负极的电极反应式:__________________________。
(3)如图是一个电解过程示意图。

①锌片上发生的电极反应式是:_______________________
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。

已知:①-CH2CN
| NaOH |
| 水溶液△ |
| 自动脱水 |
完成下列填空:
(1)反应Ⅰ的反应类型是
(2)写出结构简式.A
(3)写出D→E的化学反应方程式
(4)与M有相同的官能团的M的同分异构体共有
(5)用于纸张涂膜等的S.B.R乳胶,是由M、苯乙烯、1,3-丁二烯共聚生成,写出该乳胶的结构简式


(6)实验室用2%的硝酸银溶液和2%的氨水配制银氨溶液.简述银氨溶液的配制过程
I.已知:反应




请回答:
 反应生成气态水的热化学方程式__________________________
反应生成气态水的热化学方程式__________________________
II.实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:
它所对应的化学方程式为:_________________________________________________
(2)已知在400℃时,反应

 =0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应
=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应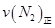 ____________
____________ (填:>、<、=、不能确定);
(填:>、<、=、不能确定);
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,
可采取的正确措施是____________(填序号)
A.加催化剂 B.升高温度 C.缩小体积增大压强 D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:

 ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:

请完成下列问题:
①判断该反应的 ___________0(填“>”或“<”)
___________0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是___________(填序号)。
A. B.容器内压强保持不变
B.容器内压强保持不变
C.A和B的转化率相等 D.混合气体的密度保持不变
查看习题详情和答案>>