摘要:4NH3+5O24NO+6H2O CH4+2O2CO2+2H2O
网址:http://m.1010jiajiao.com/timu_id_162080[举报]
工业上制硝酸可用氨催化氧化的方法,其反应为4NH3(g)+5O2(g)?4NO(g)+6H2O△H<0.某研究小组探究当其他条件不变时,改变某一条件对上述反应的影响.下列分析正确的是( )


查看习题详情和答案>>
根据如图的装置进行实验回答下列问题:

(1)在受热的试管中,写出A处的Na2O2发生反应的化学方程式:
①
(2)被加热的铂丝处发生反应的化学方程式:
(3)B管内出现的现象:
(4)烧杯C中所发生的现象:
(5)B、C中可能发生的主要反应方程式:
查看习题详情和答案>>

(1)在受热的试管中,写出A处的Na2O2发生反应的化学方程式:
①
2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
,②2H2O+2Na2O2=4NaOH+O2↑,
2H2O+2Na2O2=4NaOH+O2↑,
.(2)被加热的铂丝处发生反应的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
(3)B管内出现的现象:
无色气体变成红棕色
无色气体变成红棕色
;(4)烧杯C中所发生的现象:
溶液变红色
溶液变红色
;(5)B、C中可能发生的主要反应方程式:
2NO+O2=2NO2
2NO+O2=2NO2
;3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.Ⅰ.氨气是一种重要化合物,在工农业生产、生活中有着重要应用.
(1)如图烧瓶中盛有Na2O2固体,分液漏斗中盛有浓氨水,利用图示仪器装置(加热及夹持固定装置均已略去)进行氨的催化氧化实验.请根据下列要求回答问题:

①请选择实验装置,按气流方向从左到右连接顺序是(填字母)
②试管B中的反应方程式为
Ⅱ.①分别将氯气和二氧化硫通入品红溶液中,可观察到红色都褪去,该过程中分别体现了氯气的
②一定条件下,向碘水中通入足量氯气,完全反应后再滴加淀粉溶液无明显现象.若原有10.0mL 1.0mol?L-1的碘水,反应中共转移了0.1mol电子,则该反应的离子方程式为:
Ⅲ.为了探究NO做催化剂参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生反应化学方程式为
查看习题详情和答案>>
(1)如图烧瓶中盛有Na2O2固体,分液漏斗中盛有浓氨水,利用图示仪器装置(加热及夹持固定装置均已略去)进行氨的催化氧化实验.请根据下列要求回答问题:

①请选择实验装置,按气流方向从左到右连接顺序是(填字母)
A
A
→D
D
→B
B
→E;②试管B中的反应方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
Ⅱ.①分别将氯气和二氧化硫通入品红溶液中,可观察到红色都褪去,该过程中分别体现了氯气的
氧化
氧化
性、二氧化硫的漂白性
漂白性
性.②一定条件下,向碘水中通入足量氯气,完全反应后再滴加淀粉溶液无明显现象.若原有10.0mL 1.0mol?L-1的碘水,反应中共转移了0.1mol电子,则该反应的离子方程式为:
5Cl2+I2+6H2O═12H++2IO3-+10Cl-
5Cl2+I2+6H2O═12H++2IO3-+10Cl-
.Ⅲ.为了探究NO做催化剂参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生反应化学方程式为
2NO+O2=2NO2
2NO+O2=2NO2
、NO2+SO2=NO+SO3
NO2+SO2=NO+SO3
,再喷射适量蒸馏水即得硫酸型酸雨.已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为75%,C、J是同周期元素的气态氢化物,X为无色液体,D具有两性.反应生成的水均已略去.它们有如下图所示的关系.

(1)写出化学式:A.
(2)反应③中每生成lmolF,转移电子的数目为:
(3)反应④的化学方程式为:
(4)写出离子方程式分别为:反应②
反应⑤
(5)反应①中,每1.00g C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式.
查看习题详情和答案>>

(1)写出化学式:A.
Al4C3
Al4C3
,B.Na2O2
Na2O2
,C.CH4
CH4
.(2)反应③中每生成lmolF,转移电子的数目为:
1.204×1024
1.204×1024
.(3)反应④的化学方程式为:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(4)写出离子方程式分别为:反应②
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-
;反应⑤
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
.(5)反应①中,每1.00g C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式.
CH4(g)+2O2(g)
CO2(g)+2H2O(l);△H=-889.6kJ?mol-1
| ||
CH4(g)+2O2(g)
CO2(g)+2H2O(l);△H=-889.6kJ?mol-1
.
| ||
依据下图中氮元素及其化合物的转化关系,请回答下列问题.
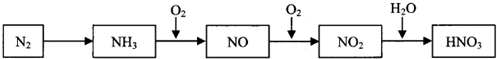
(1)实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,该反应的化学方程式是
(2)实验室检验氨气时,可选用的试剂是
a.蓝色石蕊试纸 b.红色石蕊试纸 c.浓盐酸
(3)工业上用氨气制取NO的化学方程式是
(4)NO2是一种空气污染物,将其通入Na2CO3溶液进行尾气处理,可以得到NaNO2和另外两种常见物质(其中一种为气体),这一反应的化学方程式是
查看习题详情和答案>>

(1)实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,该反应的化学方程式是
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(2)实验室检验氨气时,可选用的试剂是
bc
bc
(填字母).a.蓝色石蕊试纸 b.红色石蕊试纸 c.浓盐酸
(3)工业上用氨气制取NO的化学方程式是
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(4)NO2是一种空气污染物,将其通入Na2CO3溶液进行尾气处理,可以得到NaNO2和另外两种常见物质(其中一种为气体),这一反应的化学方程式是
2NO2+Na2CO3═NaNO2+NaNO3+CO2
2NO2+Na2CO3═NaNO2+NaNO3+CO2
.