题目内容
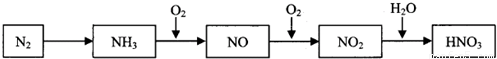
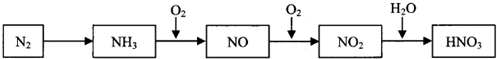
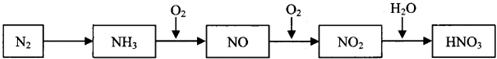
依据下图中氮元素及其化合物的转化关系,请回答下列问题.
(1)实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,该反应的化学方程式是
(2)实验室检验氨气时,可选用的试剂是
a.蓝色石蕊试纸 b.红色石蕊试纸 c.浓盐酸
(3)工业上用氨气制取NO的化学方程式是
(4)NO2是一种空气污染物,将其通入Na2CO3溶液进行尾气处理,可以得到NaNO2和另外两种常见物质(其中一种为气体),这一反应的化学方程式是

(1)实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,该反应的化学方程式是
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(2)实验室检验氨气时,可选用的试剂是
bc
bc
(填字母).a.蓝色石蕊试纸 b.红色石蕊试纸 c.浓盐酸
(3)工业上用氨气制取NO的化学方程式是
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(4)NO2是一种空气污染物,将其通入Na2CO3溶液进行尾气处理,可以得到NaNO2和另外两种常见物质(其中一种为气体),这一反应的化学方程式是
2NO2+Na2CO3═NaNO2+NaNO3+CO2
2NO2+Na2CO3═NaNO2+NaNO3+CO2
.分析:(1)氯化铵与氢氧化钙在加热条件下反应生成氯化钙、氨气与水;
(2)氨气可以是湿润的红色石蕊试纸变蓝,与氯化氢反应生成氯化铵,冒白烟,据此检验氨气;
(3)工业上利用氨气与氧气发生催化氧化生成NO与水;
(4)Na2CO3溶液进行尾气处理,可以得到NaNO2,根据电子转移守恒可知,二氧化氮还发生氧化反应,应生成硝酸,硝酸再与碳酸钠反应生成硝酸钠与二氧化碳,据此书写.
(2)氨气可以是湿润的红色石蕊试纸变蓝,与氯化氢反应生成氯化铵,冒白烟,据此检验氨气;
(3)工业上利用氨气与氧气发生催化氧化生成NO与水;
(4)Na2CO3溶液进行尾气处理,可以得到NaNO2,根据电子转移守恒可知,二氧化氮还发生氧化反应,应生成硝酸,硝酸再与碳酸钠反应生成硝酸钠与二氧化碳,据此书写.
解答:解:(1)氯化铵与氢氧化钙在加热条件下反应生成氯化钙、氨气与水,反应方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)氨气可以是湿润的红色石蕊试纸变蓝,与氯化氢反应生成氯化铵,冒白烟,据此检验氨气,
故答案为:bc;
(3)工业上利用氨气与氧气发生催化氧化制备NO,反应方程式为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(4)Na2CO3溶液进行尾气处理,可以得到NaNO2,根据电子转移守恒可知,二氧化氮还发生氧化反应,应生成硝酸,硝酸再与碳酸钠反应生成硝酸钠与二氧化碳,反应总方程式为:2NO2+Na2CO3═NaNO2+NaNO3+CO2,
故答案为:2NO2+Na2CO3═NaNO2+NaNO3+CO2.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)氨气可以是湿润的红色石蕊试纸变蓝,与氯化氢反应生成氯化铵,冒白烟,据此检验氨气,
故答案为:bc;
(3)工业上利用氨气与氧气发生催化氧化制备NO,反应方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(4)Na2CO3溶液进行尾气处理,可以得到NaNO2,根据电子转移守恒可知,二氧化氮还发生氧化反应,应生成硝酸,硝酸再与碳酸钠反应生成硝酸钠与二氧化碳,反应总方程式为:2NO2+Na2CO3═NaNO2+NaNO3+CO2,
故答案为:2NO2+Na2CO3═NaNO2+NaNO3+CO2.
点评:本题考查氨气的制备与性质、氧化还原反应等,(4)中注意利用电子转移守恒判断产物,难度中等.

练习册系列答案
相关题目
 2NH3(g)
2NH3(g)
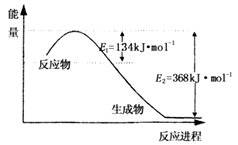
 2N2O5(g);已知体系中n(NO2)随时间变化如下表:
2N2O5(g);已知体系中n(NO2)随时间变化如下表: 
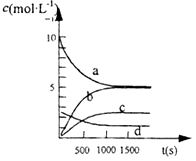
 2NH3(g)达到化学平衡状态的依据的是___________(填序号字母)。
2NH3(g)达到化学平衡状态的依据的是___________(填序号字母)。