摘要:3Cl2+2NH3N2+6HCl Si+4HFSiF4+2H2
网址:http://m.1010jiajiao.com/timu_id_162075[举报]
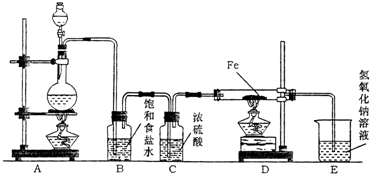 某研究性学习小组设计如图装置制取氯气并以氯气为原料进行实验.
某研究性学习小组设计如图装置制取氯气并以氯气为原料进行实验.(1)装置A烧瓶中发生反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(2)装置B中饱和食盐水的作用是
除去HCl
除去HCl
,装置C中浓硫酸的作用是吸收水蒸气
吸收水蒸气
;(3)实验时,先点燃
A
A
处的酒精灯,再点燃D
D
处酒精灯,写出D中反应的化学方程式2Fe+3Cl2=2FeCl3
2Fe+3Cl2=2FeCl3
,写出E中反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
;(4)若实验中用12mol?L-1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是:①
HCl挥发
HCl挥发
,②浓盐酸变稀不再反应
浓盐酸变稀不再反应
.欲使反应生成Cl2的物质的量最大程度的接近0.03mol,则在装置气密性良好的前提下实验中应采取的措施是
慢慢滴加浓盐酸,缓缓加热
慢慢滴加浓盐酸,缓缓加热
.