摘要:A.含20.0 g NaOH 的稀溶液与稀盐酸完全中和.放出28.7 kg的热量.则表示该反应中和热的热化学方程式为:HCl= H2O,ΔH=-57.4 kJ? mol―1B.由4P= P4,ΔH >0可知.白磷的热稳定性比红磷大C.已知2H2(g)+O2(g)=2H2O(g),ΔH=-483.6 kJ?mol-1 .则H2 的燃烧热大于241.8 kJ?mol-1D.已知:2C(g)+ 2O2(g)=2CO2(g),△H1 及:2C(s)+ O2,△H2 .则△H1 <△H2
网址:http://m.1010jiajiao.com/timu_id_142362[举报]
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
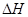 =
+28.7 kJ·mol-1
=
+28.7 kJ·mol-1
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
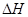 =
-28.7 kJ·mol-1
=
-28.7 kJ·mol-1
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
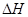 =
+57.4 kJ·mol-1
=
+57.4 kJ·mol-1
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
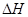 =
-57.4 kJ·mol-1
=
-57.4 kJ·mol-1
查看习题详情和答案>>
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +28.7" kJ·mol-1 =" +28.7" kJ·mol-1 |
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -28.7" kJ·mol-1 =" -28.7" kJ·mol-1 |
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +57.4" kJ·mol-1 =" +57.4" kJ·mol-1 |
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -57.4" kJ·mol-1 =" -57.4" kJ·mol-1 |
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +28.7" kJ·mol-1 =" +28.7" kJ·mol-1 |
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -28.7" kJ·mol-1 =" -28.7" kJ·mol-1 |
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +57.4" kJ·mol-1 =" +57.4" kJ·mol-1 |
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -57.4" kJ·mol-1 =" -57.4" kJ·mol-1 |