题目内容
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
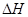 =
+28.7 kJ·mol-1
=
+28.7 kJ·mol-1
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
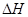 =
-28.7 kJ·mol-1
=
-28.7 kJ·mol-1
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
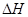 =
+57.4 kJ·mol-1
=
+57.4 kJ·mol-1
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
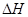 =
-57.4 kJ·mol-1
=
-57.4 kJ·mol-1
【答案】
D
【解析】
试题分析:20.0 g NaOH的物质的量为0.5mol,故1molNaOH反应放出热量为56.4kJ,方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l)
 =
-57.4 kJ·mol-1
=
-57.4 kJ·mol-1
考点:考查热化学方程式有关问题。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目