摘要:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O (2)0.448L (3)1.6mol/L
网址:http://m.1010jiajiao.com/timu_id_139080[举报]
制取硝酸铜有如下三种方案
(1)上述三种方案中最能体现绿色化学理念的是方案,理由是
(2)写出方案甲的化学方程式,并标出电子转移的方向和数目

(3)写出方案乙的离子反应方程式
查看习题详情和答案>>
| 方案编号 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
方案一、二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低
方案一、二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低
;(2)写出方案甲的化学方程式,并标出电子转移的方向和数目


(3)写出方案乙的离子反应方程式
3Cu+8H++2NO3-═Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═Cu2++2NO↑+4H2O
.(2012?天津)信息时代产生的大量电子垃圾对环境构成了极大的威胁.某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如图1制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
得到滤渣1的主要成分为
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:
上述三种方案中,
(5)探究小组用滴定法测定CuSO4?5H2O (Mr=250)含量.取a g试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol?L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2-=CuY2-+2H+
写出计算CuSO4?5H2O质量分数的表达式ω=
×100%
×100%;
下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡 c.未除净可与EDTA反应的干扰离子.
查看习题详情和答案>>

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
Cu+4H++2NO3-
Cu2++2NO2↑+2H2O 或3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O
| ||
| ||
Cu+4H++2NO3-
Cu2++2NO2↑+2H2O 或3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O
;
| ||
| ||
得到滤渣1的主要成分为
Au、Pt
Au、Pt
.(2)第②步加H2O2的作用是
将Fe2+氧化为Fe3+
将Fe2+氧化为Fe3+
,使用H2O2的优点是不引入杂质,对环境无污染
不引入杂质,对环境无污染
;调溶液pH的目的是使Fe3+、Al3+
Fe3+、Al3+
生成沉淀.(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
加热脱水
加热脱水
.(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:

上述三种方案中,
甲
甲
方案不可行,原因是所得产品中含有较多Fe2(SO4)3杂质
所得产品中含有较多Fe2(SO4)3杂质
:从原子利用率角度考虑,乙
乙
方案更合理.(5)探究小组用滴定法测定CuSO4?5H2O (Mr=250)含量.取a g试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol?L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2-=CuY2-+2H+
写出计算CuSO4?5H2O质量分数的表达式ω=
| c mol?L-1×b×10-3L×250g?mol-1×5 |
| ag |
| c mol?L-1×b×10-3L×250g?mol-1×5 |
| ag |
下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
c
c
.a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡 c.未除净可与EDTA反应的干扰离子.
(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO  2CO2+N2
2CO2+N2
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
①请在表格中填入剩余的实验条件数据.
②设计实验Ⅱ、Ⅲ的目的是
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置:
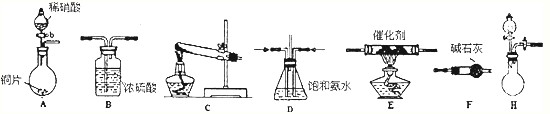
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
分析表中数据,实验室制NH3产率最高的是
步骤二、模拟尾气的处理:
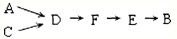
选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
③A中反应的离子方程式:
④D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:
⑤D装置中的液体可换成
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
⑥该同学所设计的模拟尾气处理实验还存在的明显缺陷是:
查看习题详情和答案>>
 2CO2+N2
2CO2+N2研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1Com] |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②设计实验Ⅱ、Ⅲ的目的是
探究温度对化学反应速率的影响
探究温度对化学反应速率的影响
.(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置:

步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:
H
H
(填装置序号).②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 | 固体试剂(g) | NH3体积(ml) | |
| a | 12.0gCa(OH)2(过量) | 10.8gNH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0gNaOH(过量) | 10.8gNH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0gCaO(过量) | 10.8gNH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |
f
f
(填序号).步骤二、模拟尾气的处理:
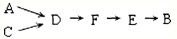
选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
③A中反应的离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.④D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:
防止氨气溶解(或防止倒吸)
防止氨气溶解(或防止倒吸)
.⑤D装置中的液体可换成
C
C
(填序号).a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
⑥该同学所设计的模拟尾气处理实验还存在的明显缺陷是:
未反应的NO无法处理,会污染环境
未反应的NO无法处理,会污染环境
.信息时代产生的大量电子垃圾对环境构成了极大的威胁.某化学兴趣小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出利用此金属混合物制备硫酸铜和硫酸铝晶体的路线:
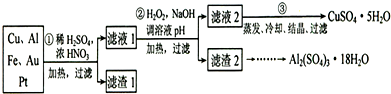
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案: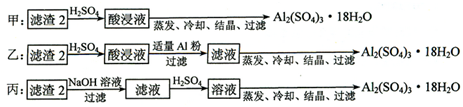
上述三种方案中,
查看习题详情和答案>>

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
Cu+4H++2NO3-
Cu2++2NO2↑+2H2O 或3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O
| ||
| ||
Cu+4H++2NO3-
Cu2++2NO2↑+2H2O 或3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O
,得到滤渣1的主要成分为
| ||
| ||
Au、Pt
Au、Pt
.(2)第②步加H2O2的作用是
将Fe2+氧化为Fe3+
将Fe2+氧化为Fe3+
,调节溶液pH的目的是使Fe3+、Al3+生成沉淀
Fe3+、Al3+生成沉淀
.(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
加热脱水
加热脱水
.(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:

上述三种方案中,
乙
乙
方案可行.某研究性学习小组设计不同实验方案来研究硝酸的性质.

实验一、甲组同学设计如图1装置来证实稀硝酸与铜反应生成NO.
(1)补充完成下列实验步骤:
①检查装置的气密性.
②打开活塞A,往U型管右侧漏斗中注入稀硝酸,一直注到
③关闭活塞A,观察实验现象.
(2)记录描述观察到的实验现象:
可观察到的现象有:U型管左侧铜丝逐渐溶解,有
(3)为了进一步证明反应确实生成的NO,还需要的操作及看到的现象为
(4)如图2的收集NO气体的各种装置中,合理的是
查看习题详情和答案>>

实验一、甲组同学设计如图1装置来证实稀硝酸与铜反应生成NO.
(1)补充完成下列实验步骤:
①检查装置的气密性.
②打开活塞A,往U型管右侧漏斗中注入稀硝酸,一直注到
稀HNO3接触到A处橡皮塞
稀HNO3接触到A处橡皮塞
为止.③关闭活塞A,观察实验现象.
(2)记录描述观察到的实验现象:
可观察到的现象有:U型管左侧铜丝逐渐溶解,有
无
无
色气体产生,溶液呈蓝色,随着反应不断进行,最后反应自行停止.该过程反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO+4H2O
3Cu+8H++2NO3-=3Cu2++2NO+4H2O
.(3)为了进一步证明反应确实生成的NO,还需要的操作及看到的现象为
打开活塞A,有红棕色气体产生
打开活塞A,有红棕色气体产生
.(4)如图2的收集NO气体的各种装置中,合理的是
CE
CE
(填选项代号).