题目内容
制取硝酸铜有如下三种方案
(1)上述三种方案中最能体现绿色化学理念的是方案,理由是
(2)写出方案甲的化学方程式,并标出电子转移的方向和数目

(3)写出方案乙的离子反应方程式
| 方案编号 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
方案一、二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低
方案一、二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低
;(2)写出方案甲的化学方程式,并标出电子转移的方向和数目


(3)写出方案乙的离子反应方程式
3Cu+8H++2NO3-═Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═Cu2++2NO↑+4H2O
.分析:(1)方案的选择要从操作是否简单、有无污染、节约原料、是否可行等方面考虑;
(2)方案甲是铜与浓硝酸的反应,根据单线桥法标出电子的转移方向和数目;
(3)方案乙是铜与稀硝酸的反应,写出反应的离子方程式即可.
(2)方案甲是铜与浓硝酸的反应,根据单线桥法标出电子的转移方向和数目;
(3)方案乙是铜与稀硝酸的反应,写出反应的离子方程式即可.
解答:解:(1)选择方案时要考虑是否产生有害气体污染空气,方案是否可行,是否安全,操作是否简单,是否节约了原料.方案一、二的生成物会污染环境,并且制取相同质量的硝酸铜,方案三消耗的原料最少,
故答案为:方案一、方案二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低;
(2)方案甲是铜与浓硝酸的反应,根据单线桥法标出电子的转移方向和数目为:

故答案为:
 ;
;
(3)铜与稀硝酸反应生成硝酸铜与一氧化氮,反应的离子方程式为:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O.
故答案为:方案一、方案二的生成物会污染环境,制取等质量的硝酸铜方案三的成本最低;
(2)方案甲是铜与浓硝酸的反应,根据单线桥法标出电子的转移方向和数目为:

故答案为:
 ;
;(3)铜与稀硝酸反应生成硝酸铜与一氧化氮,反应的离子方程式为:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O.
点评:本题考查了实验方案的评价及氧化还原反应电子转移表示方法,注意绿色化学反应要考虑是否污染,是否节约原料,本题难度中等.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
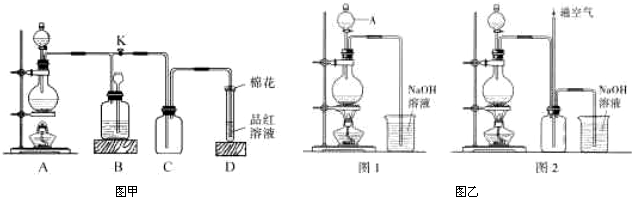


 (1)该方法中金属铜应在 (填仪器名称)中灼烧。
(1)该方法中金属铜应在 (填仪器名称)中灼烧。  方法三:
方法三: CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。
CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。