摘要:25.15g含有铜的粗锌与100g稀硫酸恰好完全反应.产生0.4g H2.(锌与稀硫酸反应的化学方程式:Zn+H2SO4==ZnSO4+H2↑铜与稀硫酸不反应)(1)求粗锌中铜的质量(2)求反应后所得溶液中生成物的质量分数.陕西师大附中2007―2008学年度第一学期期末考试九年级化学答题纸题号12345678答案 题号910111213141516答案 得分 阅卷人 得分 阅卷人
网址:http://m.1010jiajiao.com/timu_id_131261[举报]
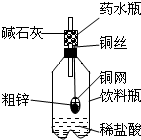 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告(1)实验目的:测定
(2)实验用品:托盘天平、药水瓶、铜网、铜丝、饮料瓶、粗锌、稀盐酸、碱石灰(CaO与Na0H的混合物).
(3)实验步骤:
| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为 粗锌的纯度为 |
①该实验中碱石灰的作用是
②若只将粗锌换成石灰石,原实验方案能否用于石灰石样品纯度的测定
③若将图中药水瓶改成直导管、粗锌换成纯锌,用原方案测定锌的相对原子质量,则结果
某实验小组在测定黄铜(铜和锌的合金)组成时,甲、乙、丙、丁四位同学分别取质量相等的黄铜样品与一定量的稀硫酸反应,所得数据记录如下表所示:
试分析计算:
(1)在乙同学测得的数据中, 已反应完全(填写物质的名称).
(2)黄铜样品中含有铜的质量分数是多少? 查看习题详情和答案>>
试分析计算:
| 样 品 | 甲 | 乙 | 丙 | 丁 |
| 黄铜样品质量/g | 50 | 50 | 50 | 50 |
| 稀硫酸的质量/g | 20 | 40 | 60 | 80 |
| 产生气体质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
(2)黄铜样品中含有铜的质量分数是多少? 查看习题详情和答案>>