摘要:1.考试大纲的修订与说明
网址:http://m.1010jiajiao.com/timu_id_127431[举报]
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验.请回答下列问题:

(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 .
(2)实验过程中,装置C中发生的现象是 ,说明SO2具有 (填“氧化性”或“还原性”).
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:
(4)尾气可采用足量 (填化学式)溶液吸收,有关反应的离子方程式是 .
(5)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题.请你推测可能的原因并说明相应的验证方法(写出一种即可): 查看习题详情和答案>>

(1)装置A中盛放亚硫酸钠的仪器名称是
(2)实验过程中,装置C中发生的现象是
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:
(4)尾气可采用足量
(5)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题.请你推测可能的原因并说明相应的验证方法(写出一种即可): 查看习题详情和答案>>
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.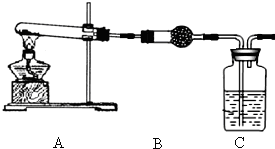
甲同学认为沉淀可能是CuCO3;乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物.(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)乙同学的观点,你认为其原理是
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗涤干净的方法是
Ⅱ.请用右图所示装置,选择必要的试剂,定性探究生成物的成分.
(3)B装置中试剂的化学式是
(4)能证明乙同学观点正确的实验现象是
(5)若丙同学的观点正确,用上述装置通过B、C中质量的增加来定量测定沉淀的组成(装置B、C中的试剂与定性探究的可以不同),请你说说该装置主要存在的缺点
查看习题详情和答案>>

甲同学认为沉淀可能是CuCO3;乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物.(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)乙同学的观点,你认为其原理是
CO32-水解成碱性,Cu2+与OH?结合生成Cu(OH)2
CO32-水解成碱性,Cu2+与OH?结合生成Cu(OH)2
;(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗涤干净的方法是
取最后一次洗涤液,滴加BaCl2溶液,无沉淀生成,说明已洗净
取最后一次洗涤液,滴加BaCl2溶液,无沉淀生成,说明已洗净
.Ⅱ.请用右图所示装置,选择必要的试剂,定性探究生成物的成分.
(3)B装置中试剂的化学式是
CuSO4
CuSO4
,C装置中试剂的名称是澄清石灰水
澄清石灰水
.(4)能证明乙同学观点正确的实验现象是
B中无水硫酸铜变蓝,C澄清石灰水不变浑浊
B中无水硫酸铜变蓝,C澄清石灰水不变浑浊
.(5)若丙同学的观点正确,用上述装置通过B、C中质量的增加来定量测定沉淀的组成(装置B、C中的试剂与定性探究的可以不同),请你说说该装置主要存在的缺点
装置中原有的空气有影响,实验结束后装置中残留的气体不能被吸收,石灰水可能会吸收空气中的CO2等
装置中原有的空气有影响,实验结束后装置中残留的气体不能被吸收,石灰水可能会吸收空气中的CO2等
(至少二点).Jerry Woodall教授在实验室中,清洗一个含有液态镓、铝合金的坩埚时,偶然地发现当液态合金中的铝与水接触时,它们之间发生了反应,使水爆裂开,并产生氢气和铝的氧化物,镓在反应中不被消耗.下列说法正确的是( )
| A、铝元素、镓元素均位于第ⅢA族 | B、上述现象说明铝的还原性比镓强 | C、铝与水反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑ | D、与水反应生成的铝的氧化物,在高温下熔融,用氢气还原可制得铝 |
(2012?山东模拟)资料显示:“氨气可在纯氧中安静燃烧…某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验.

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式
②停止反应后,立即关闭B中两个活塞.一段时间后,将试管浸入冰水中.试管内气体颜色变浅,请结合化学方程式说明原因
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是
②氨气燃烧的化学方程式是
查看习题详情和答案>>

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
(NH4)2CO3或NH4HCO3
(NH4)2CO3或NH4HCO3
;碱石灰的作用是吸收水和二氧化碳
吸收水和二氧化碳
.(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;试管内气体变为红棕色,该反应的化学方程式是
| ||
| △ |
2NO+O2═2NO2
2NO+O2═2NO2
.②停止反应后,立即关闭B中两个活塞.一段时间后,将试管浸入冰水中.试管内气体颜色变浅,请结合化学方程式说明原因
2NO2?N2O4 △H<0,降温平衡向正反应方向移动,颜色变浅
2NO2?N2O4 △H<0,降温平衡向正反应方向移动,颜色变浅
.(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是
先通O2,后通NH3
先通O2,后通NH3
;其理由是若先通NH3,氨气在空气中不能燃烧,逸出造成环境污染
若先通NH3,氨气在空气中不能燃烧,逸出造成环境污染
②氨气燃烧的化学方程式是
4NH3+3O2
2N2+6H2O
| ||
4NH3+3O2
2N2+6H2O
.
| ||