摘要:32.[化学――物质结构与性质]
网址:http://m.1010jiajiao.com/timu_id_109526[举报]
【化学-物质结构与性质】
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
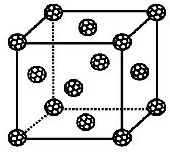
 (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
查看习题详情和答案>>
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
同位素
同位素
.Ti元素在元素周期表中的位置是第四
四
周期,第IVB
IVB
族;基态原子的电子排布式为Is22s22p63S23p63d24s2(或[Ar]3d24s2)
Is22s22p63S23p63d24s2(或[Ar]3d24s2)
按电子排布Ti元素的元素周期表分区中属于d
d
区元素. (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是BaTiO3
BaTiO3
.(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
极性共价键(或共价键)、配位键
极性共价键(或共价键)、配位键
,该配合物的配体是H2O、Cl-
H2O、Cl-
. 【化学-物质结构与性质】
【化学-物质结构与性质】已知a、b、x、y、z五种元素的原子序数依次增大,其中a原子的半径是所有原子中半径最小的,b原子中的电子有6种不同的运动状态,y原子的L层有2对成对电子,z元素的电负性是前四周期中最小的.
(1)x、y两种元素的第一电离能的大小为x
(2)固体物质M的化学式为xa5,它的所有原子最外层都符合相应的稀有气体原子的最外电子层结构.则该化合物中a元素的化合价为
(3)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,z原子可作为容体掺入C60 晶体的空隙中,形成具有良好的超导性的掺杂C60 化合物.现把C60抽象成质点,该晶体的晶胞结构如图所示,若每个四面体空隙填入一个z元素的原子,则 z元素全部填满C60 晶体的四面体空隙后,所形成的掺杂C60 化合物的化学式为
【化学--物质结构与性质】
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E的原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是 ,A、B、C、D的第一电离能由小到大的顺序为 ;
(2)B的氧化物的熔点远高于D的氧化物的熔点,理由是 ;
(3)A的最高价含氧酸根离子中,其中心原子是 杂化,D的低价氧化物分子的空间构型是 ;
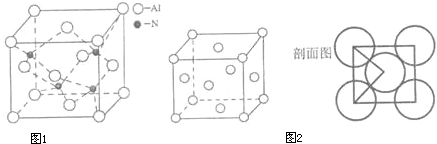
(4)A、C形成某种化合物的晶胞结构如图1所示,则其化学式为 ;(每个球均表示1个原子)
(5)铜晶体的晶胞结构如图2,若铜原子的半径是rcm,则铜的密度的计算式是 (用NA表示阿伏伽德罗常数).
查看习题详情和答案>>
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E的原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)

(1)E的核外电子排布式是
(2)B的氧化物的熔点远高于D的氧化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子是
(4)A、C形成某种化合物的晶胞结构如图1所示,则其化学式为
(5)铜晶体的晶胞结构如图2,若铜原子的半径是rcm,则铜的密度的计算式是
 【化学--物质结构与性质】
【化学--物质结构与性质】物质结构理论有助于人们理解物质变化的本质,进行分子设计和研究反应规律.请回答下列问题:
(1)第三周期基态原子有2个未成对电子且电负性最大的元素是
(2)金属晶体受到外力作用时易发生形变,而离子晶体容易破裂.试从结构的角度分析其中的主要原因
(3)已知在水中存在平衡2H2O?H3O++OH-.下列分子中,中心原子采取的杂化方式与H3O+中氧原子的杂化方式相同的是
a.CH2═CH2中的碳原子 b.NH
- 2 |
- 3 |
- 2 |
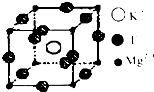
(4)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中Mg元素的质量分数为