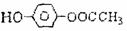22.在实验室里可用下图所示装置制取氯酸钾、次氯钾钠和探究氯水的性质。
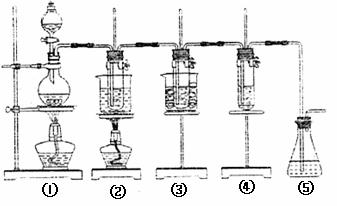
图中:①为氯气发生装置;②的试管里盛有15mL 30%KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,向烧瓶中加入适量浓盐酸的操作是 。
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是: 。
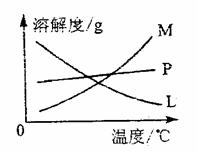
反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验名称)。
(3)本实验中制取氯酸钾的离子方程式是 。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液晨初从紫色逐渐变为 色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
|
|
然后溶液从无色逐渐变为 色 |
|
21.某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下方案:
|
|
操作 |
预测现象并做出结论 |
|
甲 |
分别将硫酸滴在火柴梗上 |
变黑者为浓硫酸 |
|
乙 |
分别加入小块金属铝片 |
产生刺激性气味者为浓硫酸 |
|
丙 |
分别加入到盛水的试管中 |
放热者为浓硫酸 |
|
丁 |
分别用玻璃棒蘸浓氨水靠近酸的瓶口 |
冒白烟者为浓硫酸 |
|
戊 |
分别加到CuSO4·5H2O晶体中 |
晶体表面由蓝变白者为浓硫酸 |
(1)其中可行的是 。
(2)其中一个稍作改进就能成为可行的是 ,改进方法是 。
(3)完全错误的是 ,因为 。
(4)用98%(ρ=1.84g/mL)的浓硫酸配制4.60mol/L的稀硫酸100mL,则应用量筒量取98%的浓硫酸的体积是 mL
20.a mol FeS与b mol FeO投入到VL、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 ( )
A.(a+b)×63g B.(a+b)×189g C.(a+b)mol D.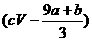 mol
mol
|
|