0 31470 31478 31484 31488 31494 31496 31500 31506 31508 31514 31520 31524 31526 31530 31536 31538 31544 31548 31550 31554 31556 31560 31562 31564 31565 31566 31568 31569 31570 31572 31574 31578 31580 31584 31586 31590 31596 31598 31604 31608 31610 31614 31620 31626 31628 31634 31638 31640 31646 31650 31656 31664 447348
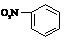 3.下列化学用语表示正确的是
3.下列化学用语表示正确的是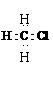 A.乙烯的结构简式:CH2CH2 B.硝基苯的分子式:
A.乙烯的结构简式:CH2CH2 B.硝基苯的分子式: 2H2+O2 2CO+O2
2H2+O2 2CO+O2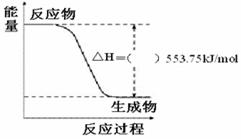
 CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表:
CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表: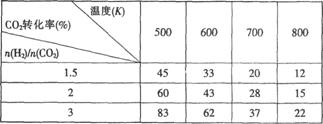

 ,其中B物质的正反应速率
,其中B物质的正反应速率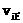 逆反应速率
逆反应速率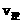 随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________
随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________