网址:http://m.1010jiajiao.com/timu3_id_93133[举报]
如图,根据下列装置回答问题:
(装置图用序号表示)
(1)写出编号①②的仪器名称:
①________________;②________________.
(2)双氧水(H2O2)是无色液体,可发生如下化学反应:
2H2O2=2H2O+O2↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是________.
(3)实验室用大理石和稀盐酸反应制取二氧化碳,在生成的气体中常混有少量氯化氢和水蒸气.C装置用于除掉水蒸气,可选用________作干燥剂(填名称).
根据下列各备选试剂的性质,利用D装置除掉氯化氢时,应选择的最佳试剂是________(填序号).
①饱和石灰水 ②氢氧化钠溶液 ③碳酸钠溶液 ④饱和碳酸氢钠溶液备选试剂的相关性质补充如下:
2NaOH+CO2=Na2CO3+H2O
Na2CO3+H2O+CO2=2NaHCO3
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
(4)将制取二氧化碳的装置按发生、净化和收集的顺序进行连接,装置依次为________(填装置序号),生成的气体通过净化装置导管口的先后顺序是________(填导管口序号).
(5)下列反应可使用A装置进行实验的是________(填序号).
①氢气还原氧化铜 ②木炭粉还原氧化铜 ③一氧化碳还原CuO
查看习题详情和答案>>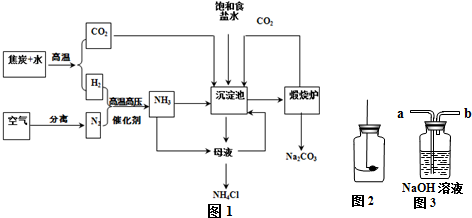
(1)该方法所用的起始原料有
(2)从空气中分离氮气有两种方法:
①物理方法:根据空气中各成分的
②化学方法:将空气中的O2与碳作用生成CO2,除去CO2后得N2.某同学在实验室中完成上述分离.先在(图2)装置中使足量的碳充分燃烧后.将得到的气体从
③利用物质间某些性质的差异选用不同的方法将它们分离.是分离物质的基本思路.请列举一种你所知道的利用物质性质差异分离物质的方法
(3)氮气与氢气化合生成氨气的化学方程式为
A.氮气与氢气不能直接化合.使用催化剂使之可以化合
B.氮气与氢气反应很慢.使用催化剂可以加快反应速率
C.催化剂在反应的前后质量和化学性质不会改变
D.根据不同的需求.人们需要控制反应条件加快或减缓反应的发生
(4)沉淀池中得到的沉淀是指
(5)根据如表列出的氯化铵和氯化钠在不同温度下的溶解度.你认为欲从母液中提取氯化铵应控制温度在
| 温度 | NH4Cl | NaCl |
| 0℃ | 29.4g | 35.6g |
| 10℃ | 33.3g | 35.8g |
| 20℃ | 37.2g | 36.0g |
| 30℃ | 41.4g | 36.6g |
| 40℃ | 45.8g | 37.0g |
根据下列装置图回答问题(装置图用符号表示)

(1)写出编号①②的仪器名称:① ②
(2)双氧水(H2O2)是无色液体,可发生如下化学反应:2H2O2 MnO2 2H2O+ O2 ↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是: 。
(3)实验室用大理石和盐酸反应制取二氧化碳,在生成的气体中混有少量氯化氢和水蒸气。C装置可用于除掉水蒸气,可选用 作干燥剂(填名称)。根据下列各备选试剂的性质,利用D装置除掉氯化氢时,应选择的最佳试剂是: (填序号)①饱和石灰水 ②氢氧化钠溶液 ③碳酸钠溶液 ④饱和碳酸氢钠溶液
备选试剂的相关性质补充如下:
2NaOH + CO2 Na2CO3 + H2O Na2CO3 + H2O + CO2 2NaHCO3
Na2CO3 + 2HCl 2NaCl + H2O + CO2↑ NaHCO3 + HCl NaCl + H2O + CO2↑
(4)将制取二氧化碳的装置按发生、净化和收集的顺序进行连接,装置依次为 (填装置序号),生成的气体通过净化装置导管口的先后顺序是: (填导管口序号)。
查看习题详情和答案>>(1)根据下图(A~E)所给的装置,实验室用高锰酸钾制取氧气,高锰酸钾固体一般放在

(2)在实验室中,集气瓶被称做“万能瓶”,用它可以组装成各种用途的装置,请仔细观察下列(F~K)各个装置的特点回答问题:

①实验室若用F装置收集氧气,则氧气应从
②若要收集一定体积
③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯

Ⅰ.写出仪器①的名称是
Ⅱ.实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式
| ||
| △ |
| ||
| △ |
②若各装置的连接顺序是:a→b→c→d,H装置内导管(“b”或“c”)该怎样延伸?请画出


③根据氯酸钾的质量算出的氧气体积为理论值.如果实际测得氧气的体积大于理论值(水的体积测量准确),你认为原因是
Ⅲ.某兴趣小组为了选择实验室制取二氧化碳的原料,对影响盐酸与大理石(大理石中杂质不与盐酸反应)反应的速率快慢的因素展开研究.
提出假设:盐酸与大理石反应的速率快慢与所用HCl的质量分数、大理石颗粒大小有关.
实验设计与实施:
| 实验编号 | 温度 | 5克大理石(碳酸钙纯度相同)规格 | 20克HCl的质量分数 | 完全反应所需时间/s |
| 实验① | 20℃ | 粗颗粒 | 20% | 140 |
| 实验② | 20℃ | 粗颗粒 | 10% | 220 |
| 实验③ | 20℃ | 细颗粒 | 20% | 30 |
写出上述实验中反应的化学方程式
实验①与②的目的是为了探究
实验
实验结论:HCl质量分数越大,反应越快;固体的颗粒越小,反应越快.
拓展与反思:还有哪些因素可能影响该反应的速率快慢呢?请写出你的一个猜想:
根据上述实验探究,实验室选用块状大理石与稀盐酸制取二氧化碳,选用上图中具有启普发生器原理的
Ⅳ.实验室在常温下用块状电石固体与水反应制取乙炔气体,该反应必须严格控制加水速度,以免剧烈反应引起发生装置炸裂;乙炔是一种微溶于水且密度比空气略小的气体.上图中制取较纯乙炔的最适宜发生和收集装置是