摘要:四种短周期元素在周期表中的相对位置如下所示.其中Z元素原子核外电子总数是其最外层电子数的3倍. X Y Z W 请回答下列问题: (1)元素Z位于周期表中第 周期. 族, (2)这些元素的氢化物中.水溶液碱性最强的是 , (3)XW2的电子式为 , (4)Y的最高价氧化物的化学式为 , (5)W和Y形成的一种二元化合物具有色温效应.请相对分子质量在170-190之间.且W的质量分数约为70%.该化合物的化学式为 . [答案]NH3,(3),(4)N2O5,(5)S4N4 命题立意:周期表.律.物质相关结构与性质的关系考查.即常说的“位构性 考查. 解析:由题干先推导出Z元素为磷元素.则X.Y.W分别是C.N.S.(3)小题的电子式教材中没有.得由二氧化碳的结构类比而来.: N(N)=≈1:1.再由相对分子质量得分子式为S4N4 [技巧点拨]“位构性 考查的题.要先找到突破口.如本题中的磷元素.再由此逐个突破.但在写教材中没出现过的元素性质.分子结构等方面的题时.可由同族元素的相似性类比.
网址:http://m.1010jiajiao.com/timu3_id_86256[举报]
 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( )| A、原子半径Z<M | B、Y的最高价氧化物对应水化物的酸性比X的弱 | C、非金属性:X<Z | D、M元素最高价氧化物对应水化物具有两性 |
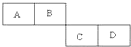 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.(1)B在元素周期表中位于
(2)A与氢元素可以形成很多化合物,在这些化合物中都含有
(3)Na 2C溶液呈碱性,其原因是
(4)用石墨电极电解NaD溶液,阴极产物是
(5)一定温度下,在密闭容器内A的单质与水蒸气发生反应生成水煤气,水蒸气的浓度变化如下图:
反应达到平衡时的平均反应速率v=

(6)B的一种氢化物B2H4可在氧气中燃烧,可制成燃料电池,电解质溶液是KOH溶液.该电池的正极的电极反应式是
V、W、X、Y、Z是五种常见元素,其中V、W、X、Y四种短周期元素在周期表中的位置如图1所示: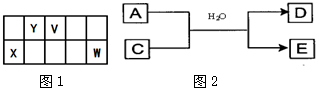
V、W的最简单气态氢化物M、N混合时有白烟生成,M能使湿润的pH试纸变蓝.Z是人体血红蛋白中存在的金属元素.请填写下列空白:
(1)W的原子结构示意图为
 ;
;
(2)二氧化钛(TiO2)与X的单质、Y的单质高温下反应只生成两种化合物,这两种化合物均由两种元素组成.其反应的化学方式
(3)含X元素的一种化合物A与Y的最高价氧化物C之间有如图2的反应关系:若E为白色沉淀,则E物质的化学式为
(4)含同价态X、Z简单离子的溶液中滴加NaOH溶液,X、Z两元素分别沉淀,X(OH)n完全沉淀的pH是4.7,Z(OH)n完全沉淀的pH是2.8,则ksp〔X(OH)n〕
(5)联氨(N2H4)也叫做肼,是重要的火箭燃料.以次氯酸钠溶液氧化M,能获得肼的稀溶液.其反应的离子方程式为
查看习题详情和答案>>

V、W的最简单气态氢化物M、N混合时有白烟生成,M能使湿润的pH试纸变蓝.Z是人体血红蛋白中存在的金属元素.请填写下列空白:
(1)W的原子结构示意图为


(2)二氧化钛(TiO2)与X的单质、Y的单质高温下反应只生成两种化合物,这两种化合物均由两种元素组成.其反应的化学方式
4Al+3TiO2+3C
2Al2O3+3TiC
| ||
4Al+3TiO2+3C
2Al2O3+3TiC
;
| ||
(3)含X元素的一种化合物A与Y的最高价氧化物C之间有如图2的反应关系:若E为白色沉淀,则E物质的化学式为
Al(OH)3
Al(OH)3
;(4)含同价态X、Z简单离子的溶液中滴加NaOH溶液,X、Z两元素分别沉淀,X(OH)n完全沉淀的pH是4.7,Z(OH)n完全沉淀的pH是2.8,则ksp〔X(OH)n〕
>
>
(填“>”或“<”)ksp〔Z(OH)n〕;(5)联氨(N2H4)也叫做肼,是重要的火箭燃料.以次氯酸钠溶液氧化M,能获得肼的稀溶液.其反应的离子方程式为
ClO-+2NH3=N2H4+Cl-+H2O
ClO-+2NH3=N2H4+Cl-+H2O
.同温同压下,将 a L M气体和b L N气体通入水中,若所得溶液的pH=7,则a>
>
b(填“>”或“<”或“=”). 四种短周期元素在周期表中的相对位置如图所示,其中Y的最外层电子数与质子数之比为6:8.下列叙述不正确的是( )
四种短周期元素在周期表中的相对位置如图所示,其中Y的最外层电子数与质子数之比为6:8.下列叙述不正确的是( )