摘要:2.X.Y.Z.W均为短周期元素且核电荷数依次增加.X的最外层电子数是内层电子总数的3倍.Y原子最外层只有一个电子.Z与X的核电荷数之比为3∶2.W原子的最外层电子数比次外层电子总数少1.下列有关叙述不正确的是 ( ) A.最高价氧化物对应水化物的碱性:YOH>Z(OH)2 B.氢化物的沸点:HW<H2X C.X.Y两元素形成的离子化合物中阴.阳离子个数比一定为1∶2 D.W的最高价氧化物对应水化物为HWO3 解析:据题意知.X为O.Y为Na.Z为Mg.W为Cl.故碱性:NaOH>Mg(OH)2.A正确,因H2O分子中含氢键.故沸点:HCl<H2O.B正确,O与Na可形成化合物Na2O.Na2O2.二者晶体中阴.阳离子数之比均为1∶2.C正确,氯元素的最高价氧化物对应水化物为HClO4.D错误. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_84054[举报]
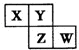 X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )| A、X、Y、Z的原子半径大小:X>Y>Z | B、Y的单质与氢气反应较Z剧烈 | C、Z、W的最高价氧化物对应水化物的酸性,前者更强 | D、X、W的气态氢化物能相互反应,生成共价化合物 |
 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的 若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )