摘要: (化学人教必修2 P93,4题)镁及其合金是一种用途很广的金属材料.目前世界上60%的镁是从海水中提取的.主要步骤如下: (1)为了使MgSO4转化Mg(OH)2,试剂①可以选用 .要MgSO4完全转化为沉淀.加入试剂①的量应 ; (2)加入试剂①后.能够分离得到Mg(OH)2沉淀的方法是 ; (3)试剂②可以选用 ; (4)无水MgCl2在熔融状态下.通电后会产生Mg和Cl2.该反应的化学方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_77370[举报]
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的.主要步骤如图:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使MgSO4完全转化为沉淀,加入试剂的量应 .
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 .
(3)试剂②选用 ;写出其反应的离子方程式 .
查看习题详情和答案>>

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②选用
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的.主要步骤如图:

(1)为了使MgSO4转化为Mg(OH)2,试剂①的物质类别为
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②的名称是
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式:
(5)生产过程中需要循环利用的物质是
查看习题详情和答案>>

(1)为了使MgSO4转化为Mg(OH)2,试剂①的物质类别为
碱
碱
,要使MgSO4完全转化为沉淀,加入试剂①的量应过量
过量
.(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
过滤
过滤
,在实验室要完成这种操作需要的玻璃仪器除了烧杯、漏斗外,还必须使用的一种仪器名称是玻璃棒
玻璃棒
,该仪器的主要作用是引流
引流
.(3)试剂②的名称是
盐酸
盐酸
.(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式:
MgCl2(熔融)
Mg+Cl2↑
| ||
MgCl2(熔融)
Mg+Cl2↑
.
| ||
(5)生产过程中需要循环利用的物质是
Cl2
Cl2
.镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的.主要步骤如下:
试回答下列问题:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②可以选用
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式
查看习题详情和答案>>
试回答下列问题:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用
Ca(OH)2
Ca(OH)2
,反应的离子方程式为Mg2++2OH-═Mg(OH)2↓
Mg2++2OH-═Mg(OH)2↓
;(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
过滤
过滤
;(3)试剂②可以选用
HCl
HCl
;(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式
MgCl2(熔融)
Mg+Cl2↑,
| ||
MgCl2(熔融)
Mg+Cl2↑,
.
| ||
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的.主要步骤如下:

(1)为了使MgSO4转化Mg(OH)2,试剂①可以选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②可以选用
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
查看习题详情和答案>>

(1)为了使MgSO4转化Mg(OH)2,试剂①可以选用
NaOH
NaOH
,要MgSO4完全转化为沉淀,加入试剂①的量应过量
过量
;(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
过滤
过滤
;(3)试剂②可以选用
盐酸
盐酸
;其反应的离子方程式为Mg(OH)2+2H+=Mg2++2H2O
Mg(OH)2+2H+=Mg2++2H2O
.(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
MgCl2(熔融)
Mg+Cl2↑
| ||
MgCl2(熔融)
Mg+Cl2↑
.
| ||
1808年,英国化学家戴维用钾还原氧化镁,最早制得少量的镁.镁是航空工业的重要材料,镁合金用于制造飞机机身、发动机零件等,一架超音速飞机约有5%的镁合金构件,一枚导弹一般消耗100~200公斤镁合金;镁作为一种强还原剂,还用于钛、锆、铍和铀等的生产中;镁是燃烧弹和照明弹不能缺少的组成物;镁粉是节日烟花必需的原料.镁及其合金是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的.从海水(主要含NaCl和MgSO4)中提取金属镁的主要步骤如图:
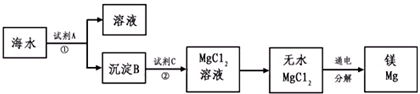
回答下列问题:
(1)Mg在周期表中的位置 ,试剂A可以选用 ,试剂C可选用 ;
(2)步骤①的离子方程式 ;
(3)用电子式表示氯化镁的形成过程 ;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为: ;
(5)戴维制镁的化学方程式为 ;
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>

回答下列问题:
(1)Mg在周期表中的位置
(2)步骤①的离子方程式
(3)用电子式表示氯化镁的形成过程
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:
(5)戴维制镁的化学方程式为
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>