摘要:15.二甲醚(CH3OCH3)被称为21世纪的新型燃料.它清洁.高效.具有优良的环保性能.四川是利用天然气生产二甲醚的重要基地之一. 请填写下列空白: (1)与二甲醚相对分子质量相等且元素种类相同的有机物的结构简式是: . (2)二甲醚可由合成气(CO+H2)在一定条件下制得.用合成气制二甲醚时.还产生了一种可参与大气循环的无机化合物.该反应的化学方程式可能是: . (3)以二甲醚.空气.氢氧化钾溶液为原料.石墨为电极可构成燃料电池.该电池中负极上的电极反应式是: . (4)制备二甲醚的合成气可由甲烷与水蒸气或二氧化碳经高温催化反应制得.合成气除制二甲醚外.还可用于冶炼金属.用它冶炼铁的生产过程可示意如下: ①在催化反应室中进行的反应均为可逆反应.增大体系的压强对甲烷转化率的影响是 (填“增大 .“减小 或“不变 ). ②在上述炼铁过程的某时间段内.若有x m3的甲烷进入燃烧室中充分燃烧.还原反应室有5y kg(即×103 mol)铁生成.假设燃烧室与还原反应室产生的高温尾气全部进入催化反应室.则这些高温尾气在理论上可产生合成气 m3.
网址:http://m.1010jiajiao.com/timu3_id_63426[举报]
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图1: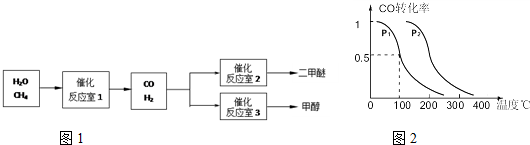
请填空:
(1)在一定条件下,反应室1中发生反应:
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0.
在其它条件不变的情况下降低温度,逆反应速率将
(2)在压强为0.1MPa条件下,反应室3(容积为2L)中0.2molCO与0.4molH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率与温度、压强的关系如图二所示,则:
①P1
②在P1压强下,100℃时,反应CO(g)+2H2(g)?CH3OH(g)的平衡常数K的值为
③在其它条件不变的情况下,反应室3再增加0.2molCO与0.4molH2,达到新平衡时,CO的转化率
查看习题详情和答案>>

请填空:
(1)在一定条件下,反应室1中发生反应:
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0.
在其它条件不变的情况下降低温度,逆反应速率将
减小
减小
(填“增大”、“减小”或“不变”).将1.0molCH4和2.0molH2O通入反应室1(假设容积为10L),1min末有0.1molCO生成,则1min内反应的平均速率v(H2)=0.03
0.03
mol?L-1?min-1.(2)在压强为0.1MPa条件下,反应室3(容积为2L)中0.2molCO与0.4molH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率与温度、压强的关系如图二所示,则:
①P1
<
<
P2 (填“<”、“>”或“=”).②在P1压强下,100℃时,反应CO(g)+2H2(g)?CH3OH(g)的平衡常数K的值为
100
100
若温度不变,再加入1.0molCO后重新达到平衡,则CO的转化率减小
减小
(填“增大”、“不变”或“减小”)③在其它条件不变的情况下,反应室3再增加0.2molCO与0.4molH2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“不变”或“减小”)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
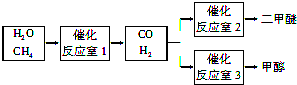
(1)写出催化反应室1中在一定条件下进行的化学反应方程式: .
(2)在压强为0.1MPa条件下,反应室3(容积为V L)中a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率与温度、压强的关系如图1所示,则
①p1 (填“<”“>”或“=”)p2.
②在其他条件不变的情况下,反应室3再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率 (填“增大”“减小”或“不变”).
③在p1压强下,100℃时,反应:CH3OH(g)?CO(g)+2H2(g)的平衡常数为 .(用含a、V的代数式表示)
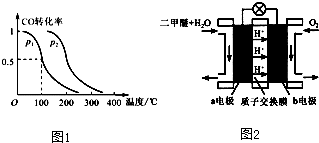
(3)图2为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为 .
(4)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ?mol-1
则反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的△H= .
查看习题详情和答案>>

(1)写出催化反应室1中在一定条件下进行的化学反应方程式:
(2)在压强为0.1MPa条件下,反应室3(容积为V L)中a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率与温度、压强的关系如图1所示,则
①p1
②在其他条件不变的情况下,反应室3再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率
③在p1压强下,100℃时,反应:CH3OH(g)?CO(g)+2H2(g)的平衡常数为

(3)图2为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为
(4)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ?mol-1
则反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的△H=
二甲醚和甲醇被称为21世纪的新型燃料,以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图1:
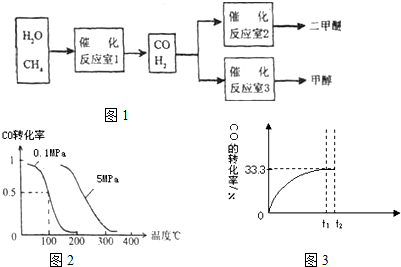
I:(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)
(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图2.
①该反应的△H
②100℃时该反应的平衡常数K=
(用含a、V的代数式表示).
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率
④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为90%,此时容器内的压强为开始时的
II:某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g).CO的转化率随时间变化关系如图2,回答下列问题:
(1)如果一个可逆反应的平衡常数K值很大,下列说法正确的是
A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应达平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应 E.该反应使用催化剂意义不大
(2)t2时刻向平衡体系中再通入1.0mol H2O(g),请在原坐标图3中将改变这一条件后CO的转化率的变化结果表示出来.
查看习题详情和答案>>

I:(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)
0.0003mo1?L-1?min-1
0.0003mo1?L-1?min-1
.(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图2.
①该反应的△H
<
<
0 (填“<”、“>”或“=”).②100℃时该反应的平衡常数K=
| V2 |
| a2 |
| V2 |
| a2 |
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“减小”或“不变”).平衡常数不变
不变
(填“增大”、“减小”或“不变”)④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为90%,此时容器内的压强为开始时的
0.55
0.55
倍.II:某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g).CO的转化率随时间变化关系如图2,回答下列问题:
(1)如果一个可逆反应的平衡常数K值很大,下列说法正确的是
C
C
(填字母).A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应达平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应 E.该反应使用催化剂意义不大
(2)t2时刻向平衡体系中再通入1.0mol H2O(g),请在原坐标图3中将改变这一条件后CO的转化率的变化结果表示出来.
(2013?浙江模拟)必考题二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:请填空:

(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为
(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
①P1
②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率
③在P1压强下,100℃时,CH3OH(g) CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为
(用含a、V的代数式表示).
查看习题详情和答案>>

(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将减小
减小
(填“增大”、“减小”或“不变”).将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=0.0003mol?L-1?min-1
0.0003mol?L-1?min-1
.(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为
2CO+4H2 CH3OCH3+H2O
CH3OCH3+H2O
 CH3OCH3+H2O
CH3OCH3+H2O2CO+4H2 CH3OCH3+H2O
CH3OCH3+H2O
. CH3OCH3+H2O
CH3OCH3+H2O(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:①P1
<
<
P2 (填“<”、“>”或“=“).②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“减小”或“不变”.下同.),平衡常数不变
不变
.③在P1压强下,100℃时,CH3OH(g)
 CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为| a2 |
| V2 |
| a2 |
| V2 |
(14分)二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
请填空:
(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H>0。
CO(g)+3H2(g)△H>0。
在其它条件不变的情况下降低温度,逆反应速率将 (填“增大”、“减小”或“不变”)。将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)= mol·L-1·min-1。
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为 。
(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g) +2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
① P1 P2 (填“<”、“>”或“=”)。
②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率______(填“增大”、“减小”或“不变”,下同。),平衡常数 。
③在P1压强下,100℃时,CH3OH(g) CO(g) + 2H2(g)反应的平衡常数为
(用含a、V的代数式表示)。
查看习题详情和答案>>